题目内容
6.甲醇是重要的化工原料,又可作为燃料.工业上可利用CO或CO2来生产燃料甲醇.已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下所示.| 化学反应 | 平衡 常数 | 温度/℃ | ||
| 500 | 700 | 800 | ||
| ①2H2(g)+CO(g)?CH3OH(g) | K1 | 2.5 | 0.34 | 0.15 |
| ②H2(g)+CO2(g)?H2O(g)+CO(g) | K2 | 1.0 | 1.70 | 2.52 |
| ③3H2(g)+CO2(g)?CH3OH(g)+H2O(g) | K3 | |||
(1)反应②是吸热(填“吸热”或“放热”)反应.
(2)据反应①与②可推导出K1、K2与K3之间的关系,则K3=K1•K2(用K1、K2表示).
(3)500℃时测得反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol•L-1)分别为0.8、0.1、0.3、0.15,则此时v正>v逆(填“>”、“=”或“<”).
(4)反应①按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图1所示.
下列说法正确的是C(填序号).
A.温度:T1>T2>T3
B.正反应速率:v(a)>v(c),v(b)>v(d)
C.平衡常数:K(a)>K(c),K(b)=K(d)
(5)新型高效的甲醇燃料电池采用铂为电极材料,两电极上分别通入CH3OH和O2.
某研究小组将两个甲醇燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图2所示.回答下列问题:
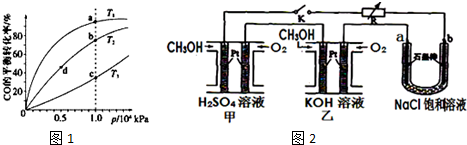
乙燃料电池的负极反应式为2CH3OH-12e-+16OH-=2CO32-+12H2O.
分析 (1)反应②CO2(g)+H2(g)?CO(g)+H2O(g)的平衡常数随温度升高增大,说明平衡正向进行,升高温度平衡向吸热方向移动;
(2)平衡常数是利用生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积,结合反应①+②得到反应③,平衡常数K3等于反应①②平衡常数的积;
(3)500℃时,测得反应③在某时刻,CO2(g)、H2(g)、CH3OH(g)、H2O(g)的浓度分别为0.1mol•L-1、0.8mol•L-1、0.3mol•L-1、0.15mol•L-1,Q=$\frac{0.3×0.15}{0.83×0.1}$=0.88,根据浓度商与化学平衡常数相对大小确定反应方向,从而确定正逆反应速率相对大小;
(4)A.根据反应①中温度与K的关系,可推断该反应为放热反应,升温,平衡左移,CO的转化率减小;
B.温度越高,化学反应速率越大,压强越大化学反应速率越大;
C.温度越高,平衡常数越小,压强对平衡常数无影响;
(5)甲醇燃料碱性电池中,负极上甲醇失电子和氢氧根离子反应生成碳酸根离子和水.
解答 解:(1)反应②CO2(g)+H2(g)?CO(g)+H2O(g)的平衡常数随温度升高增大,说明平衡正向进行,正反应是吸热反应;
故答案为:吸热;
(2)平衡常数是利用生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积,结合反应①+②得到反应③,可得平衡常数K3=K1•K2;
故答案为:K1•K2;
(3)500℃时,测得反应③在某时刻,CO2(g)、H2(g)、CH3OH(g)、H2O(g)的浓度分别为0.1mol•L-1、0.8mol•L-1、0.3mol•L-1、0.15mol•L-1,Q=$\frac{0.3×0.15}{0.83×0.1}$=0.88<K=2.5,则此时v正>v逆;
故答案为:>;
(4)A.根据反应①中温度与K的关系,可推断该反应为放热反应,升温,平衡左移,CO的转化率减小,所以T3>T2>T1,A错误;
B.T3>T2>T1,温度越高化学反应速率越大、压强越大化学反应速率越大,则反应速率v(c)>v(a),v(b)>v(d),B错误;
C.温度越高,平衡常数越小,压强对平衡常数无影响,所以K(a)>K(c),K(b)=K(d),C正确;
故选C;
(5)甲醇燃料碱性电池中,负极上甲醇失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为2CH3OH-12e-+16OH-=2CO32-+12H2O,
故答案为:2CH3OH-12e-+16OH-=2CO32-+12H2O.
点评 本题考查化学平衡计算、外界条件对化学平衡移动影响、原电池原理等知识点,侧重考查学生图象分析判断及计算能力,会根据浓度商与化学平衡常数相对大小确定反应方向,难点是电极反应式的书写,题目难度中等.

 活力课时同步练习册系列答案
活力课时同步练习册系列答案| A. | MnO4→Mn2- | B. | HCl→Cl2 | C. | Fe→Fe3- | D. | KClO3→O2 |
(1)已知:
| 化学式 | H2(g) | CO(g) | CH3OH(l) |
| 标准燃烧热(25℃) △H/kJ•mol-1 | -285.8 | -283.0 | -726.5 |
(2)在容积可变的密闭容器中充入1mol CO ( g ) 和2molH2 ( g )生成CH3OH( g ),H2的平衡转化率随温度(T)、压强(P)的变化如图1所示.
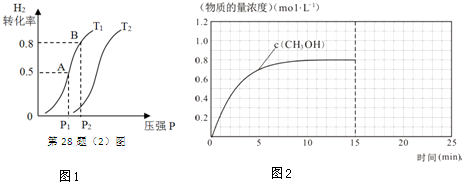
①该反应的△S<0,图中的T1<T2(填“<”、“>”或“=”).
②当达到平衡状态A 时,容器的体积为2L,此时该反应的平衡常数为4,若达到平衡状态B 时,则容器的体积V(B)=0.4L.
③在该容器中,下列措施可增加甲醇产率的是B.
A.升高温度 B.从平衡体系中及时分离CH3OH
C.充入He D.再充入0.5mol CO和1mol H2
(3)在容积固定为2L的密闭容器中充入2molCO( g )和6molH2( g )生成CH3OH( g ),反应时间与物质的量浓度的关系如图2所示,则前10分钟内,氢气的平均反应速率为0.16mol•L-1•min-1;若15分钟时升高体系温度,在20分钟时达到新平衡,此时氢气的转化率为33.3%,请在图2中画出15-25分钟c (CO)的变化曲线.
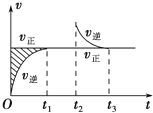 恒温密闭容器发生可逆反应:Z(?)+W(?)?X(g)+Y(?);△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列有关说法中正确的是( )
恒温密闭容器发生可逆反应:Z(?)+W(?)?X(g)+Y(?);△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列有关说法中正确的是( )| A. | Z和W在该条件下有一种是为气态 | |
| B. | t1~t2时间段与t3时刻后,两时间段反应体系中气体的平均摩尔质量不可能相等 | |
| C. | 若在该温度下此反应平衡常数表达式为K=c(X),则t1~t2时间段与t3时刻后的X浓度不相等 | |
| D. | 若该反应只在某温度T0以上自发进行,则该反应的平衡常数K随温度升高而增大 |
| A. | 醛基的结构简式-COH | B. | 聚丙烯的结构简式 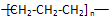 | ||
| C. | 四氯化碳分子的电子式 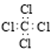 | D. | 丙烷分子的球棍模型 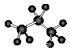 |
 以NaCl等为原料制备KClO4的过程如下:
以NaCl等为原料制备KClO4的过程如下: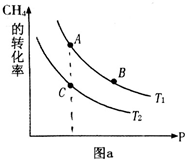 氢气、甲醇是优质的清洁燃料,可制作燃料电池.
氢气、甲醇是优质的清洁燃料,可制作燃料电池.