题目内容
一定条件下,在体积为10L的密闭容器中,2mol X和2mol Y进行如下反应:2X(g)+Y(g)?Z(g),经2min达到平衡,生成0.6mol Z.下列说法正确的是( )
| A、以X浓度变化表示的反应速率为0.06mol/(L?min) | ||
B、将容器体积变为20L,Z的平衡浓度为原来的
| ||
| C、平衡时,X的转化率为30% | ||
| D、起始状态和平衡时容器内的气体压强比为2:1 |
考点:化学平衡的计算
专题:化学平衡专题
分析:A.计算出达平衡时X浓度,利用2min内,X浓度的变化,计算X的反应速率;
B.体积扩大一倍,若平衡不移动,则Z浓度降低为原来的
,由于压强减小,化学平衡向逆反应方向移动,则Z的浓度小于原来的
;
C.根据转化率计算公式计算判断;
D.根据压强之比等于物质的量之比计算判断.
B.体积扩大一倍,若平衡不移动,则Z浓度降低为原来的
| 1 |
| 2 |
| 1 |
| 2 |
C.根据转化率计算公式计算判断;
D.根据压强之比等于物质的量之比计算判断.
解答:
解:A.达平衡后,Z物质的量为0.6mol,即生成了0.6molZ,根据计量数之比可知,X物质的量消耗了1.2mol,则浓度变化为
=0.12mol/L,其反应速率为
=0.06mol/(L?min),故A正确;
B.体积扩大一倍,若平衡不移动,则Z浓度降低为原来的
,由于压强减小,化学平衡向逆反应方向移动,则Z的浓度小于原来的
,故B错误;
C.X物质的量消耗了1.2mol,起始物质的量为2mol,转化率为
×100%=60%,故C错误;
D.反应前气体总物质的量为4mol,达平衡时,生成了0.6molZ,X物质的量为2-1.2=0.8mol,Y物质的量为2-0.6=1.4mol,气体总物质的量为0.6+0.8+1.4=2.8mol,则压强之比为
=
,故D错误;
故选A.
| 1.2mol |
| 10L |
| 0.12mol/L |
| 2min |
B.体积扩大一倍,若平衡不移动,则Z浓度降低为原来的
| 1 |
| 2 |
| 1 |
| 2 |
C.X物质的量消耗了1.2mol,起始物质的量为2mol,转化率为
| 1.2mol |
| 2mol |
D.反应前气体总物质的量为4mol,达平衡时,生成了0.6molZ,X物质的量为2-1.2=0.8mol,Y物质的量为2-0.6=1.4mol,气体总物质的量为0.6+0.8+1.4=2.8mol,则压强之比为
| 4mol |
| 2.8mol |
| 10 |
| 7 |
故选A.
点评:本题考查化学反应速率计算、化学平衡移动、转化率计算等,难度不大,其中D选项应利用阿伏伽德罗定律推论进行计算.

练习册系列答案
相关题目
室温下,将0.4mol/L HA溶液和0.2mol/LNaOH溶液等体积混合(忽略混合时溶液体积的变化)测得混合溶液的pH=5,则下列说法(或关系式)正确的是( )
| A、混合溶液中由水电离出的c(H+)=1×10-5mol/L |
| B、c(A-)+c(HA)=2c(Na+)=0.4 mol/L |
| C、c(HA)>c(A-)>c(Na+)>c(H+)>c (OH-) |
| D、c(A-)-c(HA)=2c(H+)-2 c(OH-) |
下列化学反应的速率,一定是前者大于后者的( )
| A、一定温度下,相同氢离子浓度、相同体积的盐酸与硫酸分别与大小相同的锌片反应,产生气泡的快慢 | ||||
B、反应A+B
| ||||
| C、相同温度下,与同浓度盐酸反应的锌粉和铁粉产生氢气的速率 | ||||
| D、相同温度下,颗粒大小相同的生铁分别在水和饱和食盐水中的腐蚀 |
下列过程需要通电才能进行的是( )
①电离 ②电镀 ③电解 ④电化学腐蚀 ⑤电泳.
①电离 ②电镀 ③电解 ④电化学腐蚀 ⑤电泳.
| A、①② | B、②③⑤ | C、②③ | D、全部 |
下列化工生产原理错误的是( )
①可以用电解熔融的氯化钠的方法来制取金属钠;
②可以用钠加入氯化镁饱和溶液中制取镁;
③用电冶铝时,原料是氯化铝;
④炼铁高炉中所发生的反应都是放热的,故无需加热.
①可以用电解熔融的氯化钠的方法来制取金属钠;
②可以用钠加入氯化镁饱和溶液中制取镁;
③用电冶铝时,原料是氯化铝;
④炼铁高炉中所发生的反应都是放热的,故无需加热.
| A、②③④ | B、②③ |
| C、①③ | D、①②③ |
已知葡萄糖的燃烧热是-2804kJ/mol,当它氧化生成1g水时放出的热量是( )
| A、26.0 kJ |
| B、51.9 kJ |
| C、155.8 kJ |
| D、467.3 kJ |
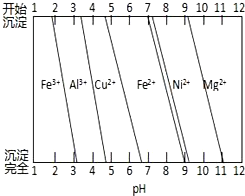 金属材料在人类生产生活中有着重要的应用,但人们使用更多的不是纯金属,而是合金.
金属材料在人类生产生活中有着重要的应用,但人们使用更多的不是纯金属,而是合金.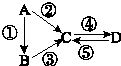 A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系:
A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系: