题目内容
设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A、常温下,17.6g丙烷中所含的极性共价键为4NA |
| B、常温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA |
| C、28g聚乙烯树脂完全燃烧时,转移的电子数目为3NA |
| D、在合成28g聚乙烯树脂的单体中,含有的双键数目为1.5NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.丙烷中的极性键为碳氢键,丙烷分子中含有8个碳氢键,17.6g丙烷的物质的量为:
=0.4mol,0.4mol丙烷中含有3.2mol极性键;
B.乙烯和丙烯的最简式为CH2,根据最简式计算出21g混合气体中含有的碳原子数目;
C.聚乙烯的最简式为CH2,根据最简式计算出消耗氧气的物质的量及转移的电子数;
D.聚乙烯为乙烯加聚反应产物,其分子中不存在碳碳双键.
| 17.6g |
| 44g/mol |
B.乙烯和丙烯的最简式为CH2,根据最简式计算出21g混合气体中含有的碳原子数目;
C.聚乙烯的最简式为CH2,根据最简式计算出消耗氧气的物质的量及转移的电子数;
D.聚乙烯为乙烯加聚反应产物,其分子中不存在碳碳双键.
解答:
解:A.丙烷的结构简式为CH3CH2CH3,丙烷分子中存在8个碳氢极性键,17.6g丙烷的物质的量为:
=0.4mol,0.4mol丙烷中含有:0.4mol×8=3.2mol极性键,所含的极性共价键为3.2NA,故A错误;
B.21.0g乙烯和丁烯的混合气体中含有1.5mol最简式CH2,含有1.5molC原子,含有的碳原子数目为1.5NA,故B正确;
C.28g聚乙烯树脂中含有2mol最简式CH2,2molCH2完全燃烧消耗3mol氧气,转移的电子的物质的量为:3mol×4=12mol,转移的电子数目为3NA,故C错误;
D.聚乙烯的结构简式为: ,聚乙烯中不存在碳碳双键,故D错误;
,聚乙烯中不存在碳碳双键,故D错误;
故选B.
| 17.6g |
| 44g/mol |
B.21.0g乙烯和丁烯的混合气体中含有1.5mol最简式CH2,含有1.5molC原子,含有的碳原子数目为1.5NA,故B正确;
C.28g聚乙烯树脂中含有2mol最简式CH2,2molCH2完全燃烧消耗3mol氧气,转移的电子的物质的量为:3mol×4=12mol,转移的电子数目为3NA,故C错误;
D.聚乙烯的结构简式为:
 ,聚乙烯中不存在碳碳双键,故D错误;
,聚乙烯中不存在碳碳双键,故D错误;故选B.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确聚乙烯的结构简式,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
请回忆食盐晶体的晶胞结构,已知食盐的密度为ρ g?cm-3,其摩尔质量为M g?mol-1,阿伏加德罗常数为NA,则在食盐晶体中Na+和Cl-的核间距大约是( )
A、
| |||||
B、
| |||||
C、
| |||||
D、
|
下列溶液中,跟100mL0.5mol?L-1NaNO3溶液所含的NO3-物质的量浓度相同的是( )
| A、100mL0.5mol?L-1Mg(NO3)2溶液 |
| B、200mL1mol?L-1Ca(NO3)2溶液 |
| C、50mL1mol?L-1NaNO3溶液 |
| D、25mL0.5mol?L-1HNO3溶液 |
下列有关化学用语使用正确的是( )
| A、乙醇的分子式:C2H5OH |
B、乙烯的比例模型: |
C、CO2的电子式: |
D、钾原子结构示意图: |
1mol丙烯与氯气完全加成后再与氯气取代,整个过程最多需氯气为( )
| A、5mol | B、6mol |
| C、7mol | D、8mol |

 (1)人们常用催化剂来选择反应进行的方向.如图所示为一定条件下1mol CH3OH与O2发生反应时,生成CO、CO2或HCHO的能量变化图[反应物O2(g)和生成物H2O(g)略去].
(1)人们常用催化剂来选择反应进行的方向.如图所示为一定条件下1mol CH3OH与O2发生反应时,生成CO、CO2或HCHO的能量变化图[反应物O2(g)和生成物H2O(g)略去].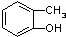 和
和 ⑥
⑥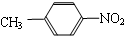 和
和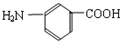
 人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格.
人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格.