题目内容
下列叙述中错误的是( )
| A、若将等量的硫蒸汽和硫固体分别完全燃烧,恢复到原状态,前者放出的热量多 |
| B、I2、SO3、固态氩都属于分子晶体 |
| C、1 molO2在反应中作氧化剂时,所得电子数一定为4NA |
| D、ag铁粉与含有H2SO4的CuSO4溶液恰好完全反应后,得到的固体为a g铜,则参与反应的CuSO4与H2SO4的物质的量之比为2:7 |
考点:反应热和焓变,阿伏加德罗常数,化学方程式的有关计算,分子晶体
专题:
分析:A、硫固体变为蒸汽的过程是吸热的过程;
B、分子晶体是分子间通过分子间作用力(包括范德华力和氢键)构成的晶体.常见的分子晶体有:所有非金属氢化物、部分非金属单质(金刚石、晶体硅等除外)、部分非金属氧化物(二氧化硅等除外)、几乎所有的酸、绝大多数的有机物晶体、所有常温下呈气态的物质、常温下呈液态的物质(除汞外)、易挥发的固态物质等;
C、根据例子:氧气和钠反应可以生成氧化钠,也可以生成过氧化钠来解答;
D、Fe先与CuSO4反应,再与H2SO4反应,根据反应的顺序和相关的量进行计算.
B、分子晶体是分子间通过分子间作用力(包括范德华力和氢键)构成的晶体.常见的分子晶体有:所有非金属氢化物、部分非金属单质(金刚石、晶体硅等除外)、部分非金属氧化物(二氧化硅等除外)、几乎所有的酸、绝大多数的有机物晶体、所有常温下呈气态的物质、常温下呈液态的物质(除汞外)、易挥发的固态物质等;
C、根据例子:氧气和钠反应可以生成氧化钠,也可以生成过氧化钠来解答;
D、Fe先与CuSO4反应,再与H2SO4反应,根据反应的顺序和相关的量进行计算.
解答:
解:A、硫固体变为蒸汽的过程是吸热的过程,等量的硫蒸汽和硫固体分别完全燃烧,恢复到原状态,前者放出的热量多,故A正确;
B、I2、SO3、固态氩都是分子间通过分子间作用力(包括范德华力和氢键)构成的晶体,属于分子晶体,故B正确;
C、氧气和钠反应可以生成氧化钠,也可以生成过氧化钠,2mol O2与金属钠反应,反应生成氧化钠电子转移4mol,生成过氧化钠电子转移2mol,O2不一定得到4NA个电子,故C错误;
D、ag铁粉为
mol,agCu为
mol,根据氧化还原顺序Fe先与CuSO4反应,再与H2SO4反应,因为
mol>
mol,
所以CuSO4反应完全,剩余Fe与H2SO4反应,
所以参加反应的CuSO4的物质的量为
mol,
参加反应的H2SO4的物质的量为(
-
)mol,
参加反应的CuSO4和H2SO4的物质的量之比为:
:(
-
)=7:1,故D错误.
故选CD.
B、I2、SO3、固态氩都是分子间通过分子间作用力(包括范德华力和氢键)构成的晶体,属于分子晶体,故B正确;
C、氧气和钠反应可以生成氧化钠,也可以生成过氧化钠,2mol O2与金属钠反应,反应生成氧化钠电子转移4mol,生成过氧化钠电子转移2mol,O2不一定得到4NA个电子,故C错误;
D、ag铁粉为
| a |
| 56 |
| a |
| 64 |
| a |
| 56 |
| a |
| 64 |
所以CuSO4反应完全,剩余Fe与H2SO4反应,
所以参加反应的CuSO4的物质的量为
| a |
| 56 |
参加反应的H2SO4的物质的量为(
| a |
| 56 |
| a |
| 64 |
参加反应的CuSO4和H2SO4的物质的量之比为:
| a |
| 64 |
| a |
| 56 |
| a |
| 64 |
故选CD.
点评:本题涉及反应热和焓变的关系、分子晶体的概念、电子转移以及方程式的计算等知识,注意知识的归纳和梳理是关键,难度中等.

练习册系列答案
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
下列物质既能跟硫酸反应,又能跟氢氧化钠溶液反应的是( )
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al.
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al.
| A、①②③④ | B、①和③ |
| C、③和④ | D、①和④ |
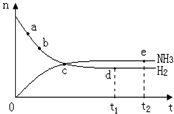 合成氨工业对国民经济和社会发展具有重要的意义,对密闭容器中的反应:
合成氨工业对国民经济和社会发展具有重要的意义,对密闭容器中的反应:N2(g)+3H2(g)
| 催化剂 |
| 高温高压 |
| A、点a的正反应速率比b点的大 |
| B、反应达到平衡时,v(N2)正=2v(NH3)逆 |
| C、点d(t1时刻)和点e(t2时刻)处n(N2)不一样 |
| D、其他条件不变,500℃下反应至t1时刻,n(H2)比图中d点值大 |
物质在反应中可表现氧化性、还原性、酸性、碱性等,下面反应的划线物质中,能在同一反应中同时表现上述两种或两种以上性质的有( )
①3FeO+10HNO3═3Fe(NO3)3+NO↑+5H2O
②C+2H2SO4(浓)═CO2↑+2SO2↑+2H2O
③8NH3+3Cl2═6NH4Cl+N2
④NaH+H2O═NaOH+H2↑
⑤2Na2O2+2H2O═4NaOH+O2↑
①3FeO+10HNO3═3Fe(NO3)3+NO↑+5H2O
②C+2H2SO4(浓)═CO2↑+2SO2↑+2H2O
③8NH3+3Cl2═6NH4Cl+N2
④NaH+H2O═NaOH+H2↑
⑤2Na2O2+2H2O═4NaOH+O2↑
| A、仅有①② | B、仅有①③④⑤ |
| C、仅有①③⑤ | D、全部 |
NA为阿伏加德罗常数的数值,下列说法中正确的是( )
| A、标准状况下,22.4 L CH3CH2OH中碳原子数为2NA |
| B、常温常压下,92g NO2和N2O4的混合气体中含有的原子数为6NA |
| C、0.2 mol?L-1 NaHCO3溶液中含Na+数为0.2NA |
| D、标准状况下,22.4L Cl2与足量的铁粉完全反应转移电子数目为3NA |
固体碘在受热时发生升华现象,有关叙述正确的是( )
| A、碘受热升华,破坏的是分子间作用力,未破坏I-I共价键,因此未发生吸热反应 |
| B、碘受热升华,吸收热量,发生了吸热反应 |
| C、碘升华,未破坏共价键,不供应热量也能发生 |
| D、碘升华过程中,热能转变为化学能 |
砒霜中毒事件时有发生,砒霜的主要成分是三氧化二砷(As2O3),医生通常给砒霜中毒患者服用一定剂量的氧化剂解毒.下列有关叙述正确的是( )
| A、砷的+3价化合物的毒性强于+5价化合物 |
| B、砷原子最外层有3个电子 |
| C、砷化氢(AsH3)比NH3稳定 |
| D、砷酸(H3AsO4)的酸性强于磷酸 |
水热法制备Fe3O4纳米颗粒的化学方程式为:3Fe++2S2O
+O2+4OH-=Fe3O4+X+2H2O.下列有关说法不正确的是( )
2- 3 |
| A、上式中的X为S4O62- |
| B、该反应中的还原剂为Fe2+和S2O32- |
| C、当生成1 mol Fe3O4时,转移电子的物质的量为4 mol |
| D、当3 mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为1 mol |