题目内容
3.下列表示分子结构的图示中,●表示短周期的几种元素的“原子实”[指原子除去最外电子层电子后剩余的部分,周围小黑点表示没有用于形成共价键的最外层电子,短线代表共价键.例如X2(X代表卤素原子):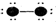
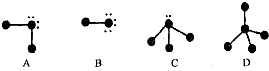
试回答下列问题:
(1)A、B、C、D四种“图示”中,所表示的物质可分为四组共8种分子.
(2)空间构型为正四面体的物质分子中,物质的稳定性顺序是CH4>SiH4;它们沸点的变化与其余各组相比不相同(填“相同”或“不相同”),其原因是其它各组中存在氢键
(3)写出上述物质中的两种间相互反应生成离子化合物的化学方程式NH3+HCl=NH4Cl.
分析 (1)先判断元素,再根据小黑点、短线表示含义书写确定化学式确定分子种类;
(2)先判断分子的空间构型,找出呈正四面体的分子,然后比较分子的稳定性,分子的沸点与分子间作用力有关,分子间存在氢键的分子其熔沸点相应升高;
(3)由阴阳离子构成的化合物是离子化合物.
解答 解:(1)A.中心原子有2个孤电子对2个共用电子对,所以是O或S元素,配原子只有1个共用电子对,所以是H元素,故化学式为H2O或H2S;
B.中心原子有3个孤电子对1个共用电子对,所以是F或Cl元素,配原子只有1个共用电子对,所以是H元素,故化学式为HF或HCl;
C.中心原子有1个孤电子对3个共用电子对,所以是N或P元素,配原子只有1个共用电子对,所以是H元素,故化学式为NH3或PH3;
D.中心原子有4个共用电子对,所以是C元素,配原子只有1个共用电子对,所以是H元素,故化学式为CH4或SiH4,;
所以A、B、C、D四种“图示”中,所表示的物质可分为四组共8种,
故答案为:8;
(2)H2O、H2S分子构型为V型,HF、HCl分子构型为直线型,NH3、PH3分子构型为三角锥型,CH4、SiH4分子构型为正四面体型,C、Si属于同一主族,其氢化物稳定性随其中心元素的非金属性从上往下依次减弱,所以物质的稳定性顺序是CH4>SiH4,H2O、HF、NH3分子间存在氢键,而CH4或SiH4没有氢键,所以它们沸点的变化与其余各组相比不相同,
故答案为:CH4>SiH4;不相同;其它各组中存在氢键;
(3)上述8种物质中,氨气和氯化氢反应NH3+HCl=NH4Cl,生成的氯化铵为铵根离子和氯离子构成的盐,属于离子化合物,
故答案为:NH3+HCl=NH4Cl.
点评 本题考查了原子最外层电子和电键图的关系,只有知道小黑点、短线表示含义结合题意才能准确判断元素,从而写出化学式,根据化学式结合物质结构有关知识分析是解答关键,注意氢键对熔沸点的影响,题目难度不大.

 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案①NaCl晶体中与每个Na+距离相等且最近的Na+共有12个
②含有共价键的晶体一定具有高的熔、沸点及硬度
③s-s σ键与s-p σ键的电子云形状相同
④含有π键的化合物与只含σ键的化合物的化学性质不同
⑤中心原子采取sp3杂化的分子,其立体构形不一定是正四面体
⑥配位键在形成时,是由成键双方各提供一个电子形成共用电子对.
| A. | ①②⑤ | B. | ①④⑤ | C. | ②③⑤ | D. | ②③⑥ |
| A. | 化学键只存在于分子内,分子间作用力只存在于分子间 | |
| B. | 冰变为液态水时,共价键没有被破坏 | |
| C. | 液态氟化氢中存在氢键,所以其分子比氯化氢稳定 | |
| D. | 物质在溶于水的过程中,化学键一定会被破坏或改变 |
| A. | 维生素C能将食物中的Fe3+转化为易吸收的Fe2+,是因为维C有氧化性 | |
| B. | SO2、NO2等在大气中达到一定浓度造成大气污染.溶液的稳定性决定了污染的长期性 | |
| C. | 燃料电池能有效提高能源的利用率是因为通过原电池装置将热能直接转化成了电能 | |
| D. | 绿色化学的核心是应用化学原理对环境污染进行有效治理 |
| A. | Al3+、NH4+、Cl?、HCO3? | B. | Na+、NO3-、SO42-、I? | ||
| C. | Na+、Mg2+、Cl?、SO42- | D. | Fe3+、K+、Cl?、NO3- |
| A. | 为了保护环境,节约资源,不使用一次性筷子、纸杯、塑料袋等 | |
| B. | 为了提高肥效、收割小麦、玉米等作物后将秸秆及时焚烧 | |
| C. | 为了提高农作物的产量和质量,应大量使用化肥和农药 | |
| D. | 为了防止干电池造成环境污染,应将废旧电池深埋处理 |
| A. | 酯化反应 | B. | 加成反应 | C. | 水解反应 | D. | 中和反应 |
 ,含有的化学键离子键、极性键.
,含有的化学键离子键、极性键.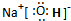 ,所含有的化学键有离子键、共价键;它属于离子化合物(填“离子”或“共价”).
,所含有的化学键有离子键、共价键;它属于离子化合物(填“离子”或“共价”).