题目内容
在Na2SO4和H2SO4的混合溶液100mL中,加入100mL 2mol/L BaCl2溶液时,恰好使SO42-全部沉淀.过滤,在滤液中加入足量锌粒,完全反应后收集到的气体为3.36L(标准状况).试计算原混合液中硫酸和硫酸钠溶液的物质的量浓度.
考点:化学方程式的有关计算
专题:计算题
分析:混合溶液加入BaCl2溶液时,发生反应:Ba2++SO42-=BaSO4↓,根据n=cV计算n(Ba2+),再根据方程式计算n总(SO42-),滤液中加入锌粒,发生反应:Zn+2H+=Zn2++H2↑,根据n=
计算氢气的物质的量,根据方程式计算n(H+),而n(H2SO4)=
n(H+),n(Na2SO4)=n总(SO42-)-n(H2SO4),再根据c=
计算.
| V |
| Vm |
| 1 |
| 2 |
| n |
| V |
解答:
解:n(Ba2+)=n(BaCl2)=0.1L×2mol/L=0.2mol,
Ba2++SO42-=BaSO4↓
1 1
0.2mol n总(SO42-)
n总(SO42-)=
=0.2mol,
标况下,3.36L氢气的物质的量=
=0.15mol,
Zn+2H+=Zn2++H2↑
2 1
n(H+) 0.15mol
n(H+)=0.15mol×2=0.3mol
n(H2SO4)=
n(H+)=0.3mol×
=0.15mol,则c(H2SO4)=
=1.5 mol/L,
n(Na2SO4)=n总(SO42-)-n(H2SO4)=0.2mol-0.15mol=0.05mol,c(Na2SO4)=
=0.5 mol/L,
答:原混合液中c(Na2SO4)=0.5 mol/L、c(H2SO4)=1.5 mol/L.
Ba2++SO42-=BaSO4↓
1 1
0.2mol n总(SO42-)
n总(SO42-)=
| 0.2mol×1 |
| 1 |
标况下,3.36L氢气的物质的量=
| 3.36L |
| 22.4L/mol |
Zn+2H+=Zn2++H2↑
2 1
n(H+) 0.15mol
n(H+)=0.15mol×2=0.3mol
n(H2SO4)=
| 1 |
| 2 |
| 1 |
| 2 |
| 0.15mol |
| 0.1L |
n(Na2SO4)=n总(SO42-)-n(H2SO4)=0.2mol-0.15mol=0.05mol,c(Na2SO4)=
| 0.05mol |
| 0.1L |
答:原混合液中c(Na2SO4)=0.5 mol/L、c(H2SO4)=1.5 mol/L.
点评:本题考查混合物计算、化学方程式计算,难度中等,明确发生的反应是关键,注意利用离子方程式解答.

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目
下列说法中正确的是( )
| A、在任何物质分子中都含有化学键 |
| B、形成离子键的阴阳离子间只存在静电吸引力 |
| C、D2O分子与H2O分子是所含电子总数不相等的分子 |
| D、CO2、PCl3分子中所有原子都满足最外层8电子稳定结构 |
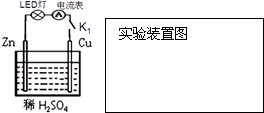 (1)原电池是一种将
(1)原电池是一种将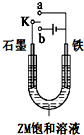 X、Y、Z、W为按原子序数由小到大排列的四种短周期元素.已知:①X可分别与Y、W形成X2Y、X2Y2、XW等共价化合物;②Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物.请回答:
X、Y、Z、W为按原子序数由小到大排列的四种短周期元素.已知:①X可分别与Y、W形成X2Y、X2Y2、XW等共价化合物;②Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物.请回答:
 依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示.请回答下列问题:
依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示.请回答下列问题: