题目内容
11.某溶液中含有大量的下列离子:Fe3+、SO42-、Al3+和M,经测定Fe3+、SO42-、Al3+和M的物质的量之比为2:4:1:1,则M可能是下列中的( )| A. | Na+ | B. | OH- | C. | Cl- | D. | S2- |
分析 根据电荷守恒判断M离子,并根据离子能否大量共存判断可能存在的离子.
解答 解:根据题目条件和电荷守恒可知:3n(Fe3+)+3n(Al3+)=2n(SO42-)+n(M),即:2×3+3×1=2×4+M,M=1,M应带有1个单位的负电荷,又OH-离子不能与Al3+、Fe3+大量共存,所以M只能为选项中的Cl-.
故选C.
点评 本题考查离子共存问题,本题的关键为根据电荷守恒判断离子的种类,题目难度不大.

练习册系列答案
相关题目
2.某有机物和过量钠反应生成气体VaL,另一份等质量的该有机物和碳酸氢钠反应生成VbL气体(同温同压),若Va=Vb,则该有机物可能是( )
| A. | HOCH2CH2COOH | B. | CH3COOH | ||
| C. | HOOC-COOH | D. | 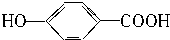 |
19.葡萄糖酸钙是一种可促进骨骼生长的营养物质.葡萄糖酸钙可通过以下反应制得:
C6H12O6(葡萄糖)+Br2+H2O→C6H12O7(葡萄糖酸)+2HBr
2C6H12O7(葡萄糖酸)+CaCO3→Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2↑
相关物质的溶解性见表:
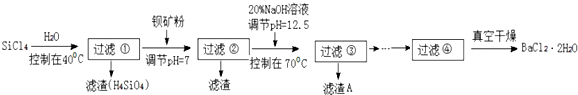
实验流程如下:

请回答下列问题:
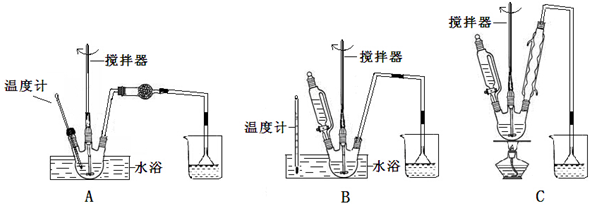
(1)第①步中溴水氧化葡萄糖时,下列装置最适合的是B.
制备葡萄糖酸钙的过程中,葡萄糖的氧化也可用其它试剂,下列物质中最适合的是C.
A.新制Cu(OH)2悬浊液 B.酸性KMnO4溶液
C.O2/葡萄糖氧化酶 D.[Ag(NH3)2]OH溶液
(2)第②步充分反应后CaCO3固体需有剩余,其目的是除去过量的溴水和将葡萄糖酸转化为葡萄糖酸钙;本实验中不宜用CaCl2替代CaCO3,理由是CaCl2不易将葡萄糖酸转化葡萄糖酸钙,也不能除去过量酸性杂质.
(3)第③步需趁热过滤,其原因是葡萄糖酸钙冷却后会结晶析出,如不趁热过滤会损失产品.
(4)第④步加入乙醇的作用是防止温度降低时,葡萄酸钙析出而损失.
(5)第⑥步中,下列洗涤剂最合适的是D.
A.冷水 B.热水 C.乙醇 D.乙醇-水混合溶液.
C6H12O6(葡萄糖)+Br2+H2O→C6H12O7(葡萄糖酸)+2HBr
2C6H12O7(葡萄糖酸)+CaCO3→Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2↑
相关物质的溶解性见表:
| 物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
| 水中的溶解性 | 可溶于冷水 易溶于热水 | 可溶 | 易溶 | 易溶 |
| 乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |

请回答下列问题:

(1)第①步中溴水氧化葡萄糖时,下列装置最适合的是B.
制备葡萄糖酸钙的过程中,葡萄糖的氧化也可用其它试剂,下列物质中最适合的是C.
A.新制Cu(OH)2悬浊液 B.酸性KMnO4溶液
C.O2/葡萄糖氧化酶 D.[Ag(NH3)2]OH溶液
(2)第②步充分反应后CaCO3固体需有剩余,其目的是除去过量的溴水和将葡萄糖酸转化为葡萄糖酸钙;本实验中不宜用CaCl2替代CaCO3,理由是CaCl2不易将葡萄糖酸转化葡萄糖酸钙,也不能除去过量酸性杂质.
(3)第③步需趁热过滤,其原因是葡萄糖酸钙冷却后会结晶析出,如不趁热过滤会损失产品.
(4)第④步加入乙醇的作用是防止温度降低时,葡萄酸钙析出而损失.
(5)第⑥步中,下列洗涤剂最合适的是D.
A.冷水 B.热水 C.乙醇 D.乙醇-水混合溶液.
3.下列的一些说法,不正确的有( )
①焰色反应是化学变化;
②干馏和分馏都属于化学变化;
③单质钠加入氯化镁溶液中制取镁;
④可以用电解熔融的氯化钠的方法来制取金属钠;
⑤用电解法制铝时,原料是氯化铝
⑥石英、玛瑙、水晶、玻璃、水泥、陶瓷、太阳能电池和光纤都是硅酸盐产品.
①焰色反应是化学变化;
②干馏和分馏都属于化学变化;
③单质钠加入氯化镁溶液中制取镁;
④可以用电解熔融的氯化钠的方法来制取金属钠;
⑤用电解法制铝时,原料是氯化铝
⑥石英、玛瑙、水晶、玻璃、水泥、陶瓷、太阳能电池和光纤都是硅酸盐产品.
| A. | ②③④⑤ | B. | ①③⑤⑥ | C. | ①②③⑤⑥ | D. | ①②③④⑤⑥ |
20.用NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 2g氢气所含原子数目为NA | |
| B. | 1.7g NH3中含N-H键数目为0.1NA | |
| C. | 标准状况下,22.4L单质溴所含有的原子数目为2NA | |
| D. | 1molMg与足量O2或N2反应生成MgO或Mg3N2均失去2NA个电子 |
1.类比归纳是学习化学的重要方法,对如下类比的说法正确的是( )
| A. | NO2、SO2都是酸性氧化物,都能使酸性高锰酸钾溶液褪色 | |
| B. | MgO、Al2O3都是高熔点离子化合物,都能用作耐热材料 | |
| C. | CO2与SiO2化学式相似,则CO2与SiO2的物理性质也相似 | |
| D. | CuO、Fe2O3都是不溶于水的碱性氧化物,都是黑色粉末 |
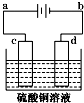 粗铜的电解精炼如图所示.在粗铜的电解过程中,粗铜板应是图中电极c(填图中的字母);在电极d上发生的电极反应式为Cu2++2e-═Cu.
粗铜的电解精炼如图所示.在粗铜的电解过程中,粗铜板应是图中电极c(填图中的字母);在电极d上发生的电极反应式为Cu2++2e-═Cu.