题目内容
10.用化学反应原理研究氮的氧化物和硫的氧化物有着重要的意义.(1)已知:2SO2(g)+O2(g)?2SO3(g)△H1
2NO(g)+O2(g)?2NO2(g)△H2
NO2(g)+SO2(g)?SO3(g)+NO(g)△H3
则△H3=$\frac{△{H}_{1}-△{H}_{2}}{2}$ (用△H1、△H2 表示),如果上述三个反应方程式的平衡常数分别为K1、K2、K3,则K3=$\sqrt{\frac{{K}_{1}}{{K}_{2}}}$(用K1、K2 表示).
(2)如图1所示,A是恒容的密闭容器,B是一个体积可变的充气气囊.保持恒温,关闭K2,分别将2mol NO 和1mol O2 通过K1、K3 分别充入A、B 中,发生的反应为2NO(g)+O2(g)?2NO2(g)[[不考虑2NO2(g)?N2O4(g)],起始时A、B 的体积相同均为a L.
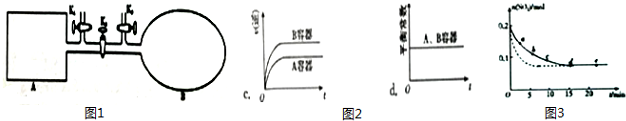
①下列说法和示意图2正确,且既能说明A容器中反应达到平衡状态,又能说明B容器中反应达到平衡状态的是a.
a.A、B 容器中气体的颜色均不再发生变化
b.A、B 容器中NO 和O2物质的量浓度比均为2:1
②T℃时,A 容器中反应达到平衡时的平衡常数Kp=8×10-2(kPa)-1.若A 容器中反应达到平 衡时p(NO2)=200kPa,则平衡时NO的转化率为66.7%. (Kp 是用平衡分压代替平衡浓=×度计算所得平衡常数,分压 总压 物质的量分数)
(3)将0.2mol SO2 和0.15mol O2通入2L 的密闭容器中,测得SO2的物质的量随时间变化如图3实线所示.
| 编号 | a | b | c | d | e |
| n(SO2)/mol | 0.16 | 0.12 | 0.09 | 0.07 | 0.07 |
| t/min | 2 | 5 | 8 | 15 | 22 |
②仅改变某一个实验条件,测得SO2 的物质的量随时间变化如图3中虚线所示,则改变的条件加入催化剂是加入催化剂.
分析 (1)①2SO2(g)+O2(g)?2SO3(g)△H1;
②2NO(g)+O2(g)?2NO2(g)△H2,
由盖斯定律可知,反应SO2(g)+NO2(g)?NO(g)+SO3(g)△H=$\frac{①-②}{2}$,如果上述三个反应方程式的平衡常数分别为K1、K2、K3,所以K3=$\sqrt{\frac{{K}_{1}}{{K}_{2}}}$;
(2)①达平衡时正逆反应速率相等,各组分的浓度保持不变的状态;
②由2NO(g)+O2(g)?2NO2(g)起始反应物投入量2mol NO 和1mol O2,设开始时NO压强为2P,O2压强为P,列三段式,根据平衡常数p(NO2)=200kPa,计算出平衡时的总压;
(3)①随着反应的进行深度逐渐减小,所以ab段平均反应速率大于bc 段平均反应速率,de 达平衡状态,浓度变化量为0;
②由图可知反应达平衡的时间缩短,而其它量不变,且仅改变某一个实验条件,所以使用催化剂.
解答 解:(1)①2SO2(g)+O2(g)?2SO3(g)△H1;
②2NO(g)+O2(g)?2NO2(g)△H2,
由盖斯定律可知,反应SO2(g)+NO2(g)?NO(g)+SO3(g)△H=$\frac{①-②}{2}$=$\frac{△{H}_{1}-△{H}_{2}}{2}$;所以K3=$\sqrt{\frac{{K}_{1}}{{K}_{2}}}$,
故答案为:$\frac{△{H}_{1}-△{H}_{2}}{2}$;$\sqrt{\frac{{K}_{1}}{{K}_{2}}}$;
(2)①a.A、B 容器中气体的颜色均不再发生变化,说明二氧化氮的浓度保持不变,达平衡状态,故正确;
b.两者起始量为2:1,变化量为2:1,所以A、B 容器中NO 和O2物质的量浓度比始终为2:1,故错误;
故选a;
②由 2NO(g)+O2(g)?2NO2(g)起始反应物投入量2mol NO 和1mol O2,设开始时NO压强为2P,O2压强为P,
开始(kPa) 2P P 0
转化(kPa)200 100 200
平衡(kPa)2P-200 P-100 200
Kp=$\frac{20{0}^{2}}{(2P-200)^{2}×(P-100)}$=8×10-2(kPa)-1,解得P=150kPa,所以则平衡时NO的转化率为:$\frac{200}{2×150}×100%$=66.7%,
故答案为:66.7%;
(3)①随着反应的进行深度逐渐减小,所以ab段平均反应速率大于bc 段平均反应速率,de 达平衡状态,浓度变化量为0,所以de 段平均反应速率为0,
故答案为:大于;0;
②由图可知反应达平衡的时间缩短,而其它量不变,且仅改变某一个实验条件,所以使用催化剂,故答案为:加入催化剂.
点评 本题考查反应热、盖斯定律的应用以及平衡常数的相关计算等,难度较大,注意平衡状态在理解及应用.

(1)配制溶液:①配制100mL1.5mol/L-1溶液,②取20mL 36.5%的盐酸稀释到200mL.配制KOH溶液时需要用的玻璃仪器有:烧杯、玻璃棒、胶头滴管和100mL容量瓶.
(2)滴定:①以酚酞作指示剂,判断到达滴定终点的实验现象是溶液由无色变为浅红色,且半分钟内不褪色.
②测定的结果如下表
| 测定次数 | 盐酸的体积/mL | KOH溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
| A. | 1.4g乙烯与丙烯的混合气体含有NA个碳原子 | |
| B. | 精炼铜,若阳极失去2NA个电子,则阴极增重64g | |
| C. | 在1L 0.1mol/L的Na2CO3溶液中,阴离子总数小于0.1NA | |
| D. | 将1L 2mol/L的FeCl3溶液加入到沸水中,加热使之完全反应,所得氢氧化铁胶体粒子数为2NA |
| A. | 6g石墨中的共价键数目 | |
| B. | 常温常压下,17g ND3中所含分子数目 | |
| C. | 0.1mol羟基(-OH)中所含电子数目 | |
| D. | 向0.2mol NH4Al(SO4)2溶液中滴加NaOH溶液至沉淀完全溶解,消耗的OH-数目 |
 15ml 0.1mol/L KOH溶液中滴入0.2mol/L(一元弱酸HA),溶液pH和加入弱酸HA体积的关系曲线如图所示,有关离子浓度的大小关系正确的是( )
15ml 0.1mol/L KOH溶液中滴入0.2mol/L(一元弱酸HA),溶液pH和加入弱酸HA体积的关系曲线如图所示,有关离子浓度的大小关系正确的是( )| A. | 在A、B间任意一点(不包括A、B两点):c(K+)>c(A-)>c(OH-)>c(H+) | |
| B. | 在B点:c(A-)=c(K+)>c(OH-)=c(H+),且a=7.5 | |
| C. | 在C点:c(A-)>c(K+)>c(OH-)>c(H+) | |
| D. | 在D点:c(A -)+c(HA)>2 c(K+) |
| A. | NH4Cl | B. | Mg(HCO3)2 | C. | H2SO4 | D. | MgCl2 |
 ),碳酸亚乙酯可由两种分子发生酯化反应制取,这两种分子的原子个数比为( )
),碳酸亚乙酯可由两种分子发生酯化反应制取,这两种分子的原子个数比为( )| A. | 3:5 | B. | 1:2 | C. | 2:3 | D. | 2:5 |
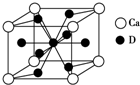 A、B、C、D是元素周期表中前36号元素,它们的核电荷数依次增大.第二周期元素A原子的核外成对电子数是未成对电子数的2倍且有3个能级,B原子的最外层p轨道的电子为半充满结构,C是地壳中含量最多的元素.D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满.请回答下列问题:
A、B、C、D是元素周期表中前36号元素,它们的核电荷数依次增大.第二周期元素A原子的核外成对电子数是未成对电子数的2倍且有3个能级,B原子的最外层p轨道的电子为半充满结构,C是地壳中含量最多的元素.D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满.请回答下列问题: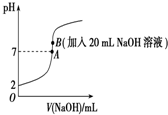 25℃下,向20mL 0.2mol•L-1的氢氟酸中滴加0.2mol•L-1的NaOH溶液时,溶液的pH变化如图所示,请回答下列问题:
25℃下,向20mL 0.2mol•L-1的氢氟酸中滴加0.2mol•L-1的NaOH溶液时,溶液的pH变化如图所示,请回答下列问题: