题目内容
14.除去下列杂质(括号内的物质),下列做法不正确的是( )| A. | NaCl固体(CaCl2):溶解,加Na2CO3溶液、过滤后加适量盐酸,最后蒸发结晶 | |
| B. | KCl固体(MnO2):溶解、过滤、蒸发结晶 | |
| C. | NaCl溶液(I2):加酒精,萃取、分液 | |
| D. | KNO3溶液(I2):加四氯化碳,萃取、分液 |
分析 A.氯化钙和碳酸钠生成碳酸钙沉淀;碳酸钠可与盐酸反应;
B.二氧化锰不溶于水,可过滤分离;
C.酒精与水混溶;
D.碘易溶于四氯化碳溶液.
解答 解:A.氯化钙和碳酸钠生成碳酸钙沉淀;过滤后碳酸钠与盐酸反应,蒸发结晶得到氯化钠,故A正确;
B.二氧化锰不溶于水,可过滤分离,蒸发结晶得到氯化钾,故B正确;
C.酒精与水混溶,不能用于萃取剂,应用苯或四氯化碳等,故C错误;
D.碘易溶于四氯化碳溶液,可用萃取的方法分离,故D正确.
故选C.
点评 本题综合考查物质的分离提纯,为高频考点,侧重于学生的分析能力和实验能力以及化学知识的综合应用,题目难度中等,注意除杂时不能引入新的杂质.

练习册系列答案
相关题目
5.下列化学用语错误的是( )
| A. | 钠的原子结构示意图: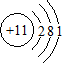 | B. | 异丁烷的结构简式: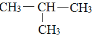 | ||
| C. | 氯化氢的电子式: | D. | 羟基的化学式:OH- |
2.某科学探究小组为探究电化学原理,设计了如图所示的装置进行探究实验.下列对实验中观察到的现象或有关结论错误的是( )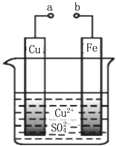

| A. | a和b不连接时,铁片上有红色的铜析出,该装置不能形成原电池 | |
| B. | a和b用导线连接时铜片为负极,发生的反应为:Cu2++2e-═Cu | |
| C. | 无论a和b是否连接,铁片均会被氧化,溶液中均有Fe2+生成 | |
| D. | a和b用导线连接时,溶液中的Cu2+应向铜电极移动 |
9.若甲烷与氯气以物质的量之比1:3混合,在光照下得到的产物:(1)CH3Cl,(2)CH2Cl2,(3)CHCl3,(4)CCl4,其中正确的是( )
| A. | 只有(1) | B. | 只有(3) | C. | (1)(2)(3)的混合物 | D. | (1)(2)(3)(4)的混合物 |
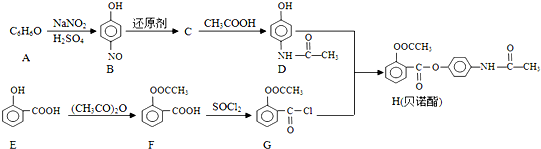
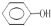 ;E中含氧官能团的名称为羟基、羧基.
;E中含氧官能团的名称为羟基、羧基.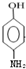 .
.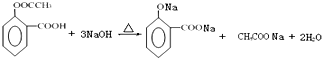 .
.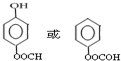 .
.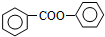 的合成路线流程图(无机试剂可任选):
的合成路线流程图(无机试剂可任选):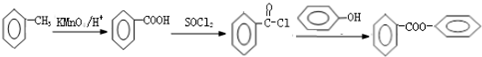 .
. 是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二.
是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二. 无色,无气味并且易燃.是常见的一种化石能源.
无色,无气味并且易燃.是常见的一种化石能源. 有强氧化性的弱酸,见光易分解,具有漂白性,可以用于消毒杀菌.
有强氧化性的弱酸,见光易分解,具有漂白性,可以用于消毒杀菌.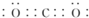 .
. ,与N3-互为等电子体的分子为N2O(写一种);
,与N3-互为等电子体的分子为N2O(写一种);