题目内容
3.下列离子在水溶液中,一定不能做氧化剂的是( )| A. | MnO4- | B. | H+ | C. | SO42- | D. | NO3- |
分析 根据化合价的高低判断物质的氧化性、还原性,最高价态的只有氧化性,最低价态的只有还原性,中间价态的既有氧化性又有还原性,以此解答该题.
解答 解:MnO4-、H+、NO3-中中心元素的化合价为最高价态,具有氧化性,SO42-在稀的酸溶液中不具有氧化性,只有在浓硫酸中具有强氧化性,
故选C.
点评 本题考查了氧化剂的判断,为高频考点,侧重考查基础知识,难度不大,根据元素的化合价判断即可,熟悉常见的氧化剂和还原剂.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
13.下列说法正确的是( )
| A. | 2Na2O2+2H2O═4NaOH+O2↑是水作还原剂的氧化还原反应 | |
| B. | 1mol Na2O2固体中含离子总数为4NA | |
| C. | 用灼烧的方法除去Na2CO3中的NaHCO3 | |
| D. | NaHCO3溶液中加入稀盐酸:CO32-+2H+═CO2↑+H2O |
14.下列离子方程式书写正确的是( )
| A. | 碳酸氢钠溶液中加稀盐酸入:HCO3-+H+═CO2↑+H2O | |
| B. | 碳酸钡和稀硝酸反应:CO32-+2H+═CO2↑+H2O | |
| C. | 铜片插入硝酸银溶液:Cu+Ag+═Cu2++Ag | |
| D. | 把金属铁放入稀硫酸中:2Fe+6H+═2Fe3++3H2↑ |
11.下列有关化学用语表示正确的是( )
| A. | N2的电子式: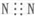 | |
| B. | S2-的结构示意图: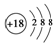 | |
| C. | 质子数为53,中子数为78的碘原子:${\;}_{58}^{131}$I | |
| D. | 乙烯的分子式:CH2=CH2 |
18.化学源于生活,又髙于生活.下列说法正确的是( )
| A. | 绿色化学的核心是在化学合成中将原子充分利用,转化为新的原子 | |
| B. | 研发使用高效催化剂,可提高反应中原料的转化率 | |
| C. | 高纯度的晶体桂可以制备晶体管等半导体、电脑芯片 | |
| D. | 酒精、NaCl溶液、CuSO4溶液、浓HNO3都可使蛋白质发生变性 |
8.下列溶液中的c(Cl-)与50mL 1mol•L-1氯化铝溶液中的c(Cl-)相等的是( )
| A. | 150 mL 1 mol•L-1氯化钠溶液 | B. | 75 mL 2 mol•L-1氯化铵溶液 | ||
| C. | 150 mL 1 mol•L-1氯化钾溶液 | D. | 75 mL 1 mol•L-1氯化铝溶液 |
12.NA表示阿伏加德罗常数,下列说法不正确的是( )
| A. | 含NA个Na+的Na2O溶解于1 L水中,Na+的物质的量浓度为1 mol•L-1 | |
| B. | 常温常压下,5.6g乙烯与丁烯(C4H8)的混合物中氢原子数为0.8NA | |
| C. | 标准状况下,4.48 LCl2与足量的Fe反应转移电子数为0.4NA | |
| D. | 0.1 mol H218O与D2O的混合物中中子数为NA |
20.一定条件下,在密闭容器中进行如下反应:NO(g)+CO(g)?$\frac{1}{2}$N2(g)+CO2(g)△H=-373.2KJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
| A. | 加催化剂同时升高温度 | B. | 加催化剂同时增大压强 | ||
| C. | 升高温度同时充入N2 | D. | 增大压强同时充入NO |