题目内容
在由水电离产生的H+浓度为1×10-11 mol/L的溶液中,一定能大量共存的离子组是( )
①K+、Cl-、NO3-、S2-; ②K+、Al3+、I-、SO42-; ③Na+、Cl-、NO3-、SO42-
④Na+、Ca2+、Cl-、HCO3- ⑤K+、Ba2+、Cl-、NO3-.
①K+、Cl-、NO3-、S2-; ②K+、Al3+、I-、SO42-; ③Na+、Cl-、NO3-、SO42-
④Na+、Ca2+、Cl-、HCO3- ⑤K+、Ba2+、Cl-、NO3-.
| A、①③ | B、②⑤ | C、③④ | D、③⑤ |
考点:离子共存问题
专题:离子反应专题
分析:常温时,若水溶液中由水电离产生的c(H+)为1×10-11mol?L-1,为酸或碱溶液,离子之间不能结合生成水、气体、沉淀等,则离子大量共存,以此来解答.
解答:
解:①NO3-和S2-在酸性溶液中不能共存,要发生氧化还原反应,故错误;
②Al3+在碱性溶液中要转化为偏铝酸根离子,故错误;
③Na+、Cl-、NO3-、SO42-无论酸或碱溶液中,该组离子之间均不反应,一定大量共存,故正确;
④Ca2+、HCO3- 在碱性溶液中要转化为碳酸钙,在酸性溶液中HCO3-要转化为二氧化碳和水,故错误;
⑤K+、Ba2+、Cl-、NO3-无论酸或碱溶液中,该组离子之间均不反应,一定大量共存,故正确;
所以③⑤正确,
故选D.
②Al3+在碱性溶液中要转化为偏铝酸根离子,故错误;
③Na+、Cl-、NO3-、SO42-无论酸或碱溶液中,该组离子之间均不反应,一定大量共存,故正确;
④Ca2+、HCO3- 在碱性溶液中要转化为碳酸钙,在酸性溶液中HCO3-要转化为二氧化碳和水,故错误;
⑤K+、Ba2+、Cl-、NO3-无论酸或碱溶液中,该组离子之间均不反应,一定大量共存,故正确;
所以③⑤正确,
故选D.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及离子之间的反应为解答的关键,侧重复分解反应的考查,注意水的电离的影响因素,题目难度不大.

练习册系列答案
相关题目
某工厂用CaSO4、NH3、H2O、CO2制备(NH4)2SO4,其工艺流程如下:
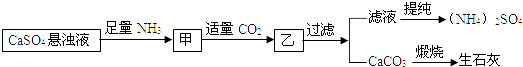
下列推断合理的是( )

下列推断合理的是( )
| A、生成lmol(NH4)2SO4至少消耗2molNH3 |
| B、上述反应过程中发生了氧化还原反应 |
| C、反应的离子方程式为:Ca2++2NH3+CO2+H2O═CaCO3↓+2NH4+ |
| D、直接蒸干滤液得到纯净的(NH4)2SO4 |
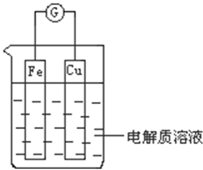 能量是一个世界性的话题,如何充分利用能量、开发新能源,为人类服务是广大科技工作者不懈努力的目标.
能量是一个世界性的话题,如何充分利用能量、开发新能源,为人类服务是广大科技工作者不懈努力的目标.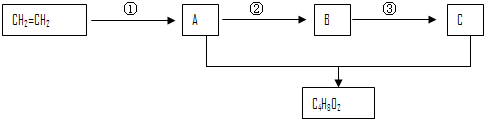
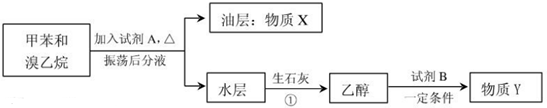
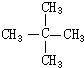 b.CH3CH2CH2CH2CH3 c.CH3CH=CHCH3 d.CH3CH=CH2
b.CH3CH2CH2CH2CH3 c.CH3CH=CHCH3 d.CH3CH=CH2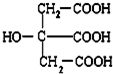
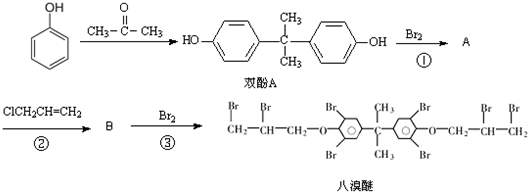
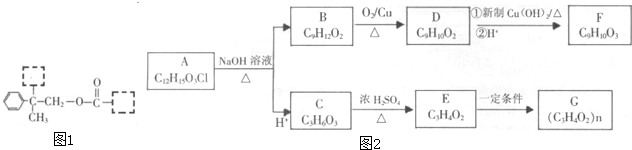
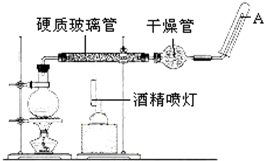 在高温下,Fe与水蒸气可发生反应.应用右边装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.请回答该实验中的问题.
在高温下,Fe与水蒸气可发生反应.应用右边装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.请回答该实验中的问题.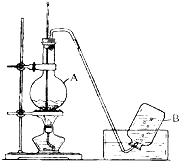 实验室用乙醇制取乙烯的装置如图,回答下列问题.
实验室用乙醇制取乙烯的装置如图,回答下列问题.