题目内容
一定量的NaHCO3和Na2CO3混合物,向其中加入500mLHCl溶液后溶液呈中性,产生标况下CO2气体4.48L,若将等量的NaHCO3和Na2CO3混合物加热后,产生气体用碱石灰吸收,碱石灰增重4.65g,则下列叙述正确的是( )
| A、加热时生成的气体在标况下3.36L |
| B、NaHCO3和Na2CO3混合物质量为17.9g |
| C、加热时若用浓硫酸吸收气体则浓硫酸增重3.3g |
| D、HCl溶液的浓度为0.6mol/L |
考点:化学方程式的有关计算,有关混合物反应的计算
专题:计算题
分析:混合物加热发生反应:2NaHCO3
Na2CO3+H2O+CO2↑,产生气体用碱石灰吸收,碱石灰增重4.65g为分解生成的二氧化碳与水的质量之和,根据水与二氧化碳的质量定比关系计算水、二氧化碳的质量,进而计算碳酸氢钠的质量,
混合物与盐酸发生反应:Na2CO3+2HCl═2NaCl+H2O+CO2↑、NaHCO3+HCl═NaCl+H2O+CO2↑,根据C元素守恒计算混合物中碳酸钠的物质的量,反应后溶液呈中性,最终为NaCl溶液,根据钠离子守恒计算n(NaCl),再根据氯离子守恒计算n(HCl),
A.加热时生成的气体在标况下的体积为二氧化碳的体积,根据n=
计算二氧化碳物质的量,再根据V=nVm计算二氧化碳的体积;
B.根据m=nM计算碳酸钠的质量,进而计算NaHCO3和Na2CO3混合物质量;
C.加热时若用浓硫酸吸收气体,则浓硫酸增重为分解生成水的质量;
D.根据c=
计算盐酸的物质的量浓度.
| ||
混合物与盐酸发生反应:Na2CO3+2HCl═2NaCl+H2O+CO2↑、NaHCO3+HCl═NaCl+H2O+CO2↑,根据C元素守恒计算混合物中碳酸钠的物质的量,反应后溶液呈中性,最终为NaCl溶液,根据钠离子守恒计算n(NaCl),再根据氯离子守恒计算n(HCl),
A.加热时生成的气体在标况下的体积为二氧化碳的体积,根据n=
| m |
| M |
B.根据m=nM计算碳酸钠的质量,进而计算NaHCO3和Na2CO3混合物质量;
C.加热时若用浓硫酸吸收气体,则浓硫酸增重为分解生成水的质量;
D.根据c=
| n |
| V |
解答:
解:混合物加热发生反应:2NaHCO3
Na2CO3+H2O+CO2↑,产生气体用碱石灰吸收,碱石灰增重4.65g为分解生成的二氧化碳与水的质量之和,由方程式可知水与二氧化碳质量之比为18:44,故生成水的质量=4.65g×
=1.35g,故二氧化碳的质量=4.65g-1.35=3.3g,故碳酸氢钠的质量=
=12.6g,
混合物与盐酸发生反应:Na2CO3+2HCl═2NaCl+H2O+CO2↑、NaHCO3+HCl═NaCl+H2O+CO2↑,标况下CO2气体4.48L,则其物质的量=
=0.2mol,混合物中NaHCO3的物质的量=
=0.15mol,根据C元素守恒,混合物中Na2CO3的物质的量=0.2mol-0.15mol=0.05mol,反应后溶液呈中性,最终为NaCl溶液,根据钠离子守恒n(NaCl)=n(NaHCO3)+2n(Na2CO3)=0.15mol+2×0.05mol=0.25mol,再根据氯离子守恒n(HCl)=n(NaCl)=0.25mol,
A.加热时生成的气体在标况下的体积为二氧化碳的体积,则二氧化碳物质的量=
=0.075mol,标况下二氧化碳的体积=0.075mol×22.4L/mol=1.68L,故A错误;
B.碳酸钠的质量=0.05mol×106g/mol=5.3g,故NaHCO3和Na2CO3混合物质量=12.6g+5.3g=17.9g,故B正确;
C.加热时若用浓硫酸吸收气体,则浓硫酸增重为分解生成水的质量,即浓硫酸增重1.35g,故C错误;
D.盐酸的物质的量浓度=
=0.5mol/L,故D错误,
故选B.
| ||
| 18 |
| 18+44 |
| 3.3g×168 |
| 44 |
混合物与盐酸发生反应:Na2CO3+2HCl═2NaCl+H2O+CO2↑、NaHCO3+HCl═NaCl+H2O+CO2↑,标况下CO2气体4.48L,则其物质的量=
| 4.48L |
| 22.4L/mol |
| 12.6g |
| 84g/mol |
A.加热时生成的气体在标况下的体积为二氧化碳的体积,则二氧化碳物质的量=
| 3.3g |
| 44g/mol |
B.碳酸钠的质量=0.05mol×106g/mol=5.3g,故NaHCO3和Na2CO3混合物质量=12.6g+5.3g=17.9g,故B正确;
C.加热时若用浓硫酸吸收气体,则浓硫酸增重为分解生成水的质量,即浓硫酸增重1.35g,故C错误;
D.盐酸的物质的量浓度=
| 0.25mol |
| 0.5L |
故选B.
点评:本题考查混合物计算,侧重学生分析思维能力的考查,注意根据方程式计算与守恒法的应用,难度中等.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
下列说法正确的是( )
| A、2mol的盐酸 |
| B、0.1mol氢 |
| C、0.3molHCl |
| D、4mol的氧元素 |
已知25℃时几种弱酸的电离平衡常数:
则下列有关说法正确的是( )
| 弱酸 | CH3COOH | HClO | H2CO3 |
| 电离平衡常数(25℃) | 1.8×10-5 | 4.7×10-8 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
| A、相同浓度的CH3COONa和NaClO的混合溶液中:C(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+) |
| B、pH相等的CH3COONa、NaClO和Na2CO3溶液:c(NaClO)<c(CH3COONa)<c(Na2CO3) |
| C、amol/L HClO溶液与bmol/L NaOH溶液等体积混合后,所得溶液中:c(Na+)>c(ClO-),则b一定大于a |
| D、向0.1mol/L CH3COOH溶液中滴加NaOH溶液至c(CH3COOH):c(CH3COO-)=5:9,此时溶液的pH=5 |
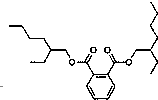 曾引起台湾地区食品安全轩然大波的塑化剂的分子结构如图所示:下列叙述中不正确的是( )
曾引起台湾地区食品安全轩然大波的塑化剂的分子结构如图所示:下列叙述中不正确的是( )| A、该物质的分子式为C24H38O4 |
| B、该物质属于酯类,不溶于水 |
| C、该物质能与溴水发生加成反应 |
| D、该物质发生水解反应,其生成的醇只有一种 |
下列叙述中,正确的是( )
| A、放热反应均能自发进行 |
| B、化学平衡发生移动,平衡常数必发生变化 |
| C、某特定反应的平衡常数仅是温度的函数 |
| D、△S为正值的反应均是自发进行的反应 |
下列电离方程式书写正确的是( )
| A、NH3?H2O=OH-+NH4+ |
| B、NaHSO4=Na++HSO4- |
| C、H2S?H++HS- |
| D、H2CO3?2H++CO32- |
下列表达方式错误的是( )
A、碳-12原子构成
| ||
B、CO2的分子模型示意图: | ||
| C、S2-的核外电子排布式 1s22s22p63s23p6 | ||
D、甲烷的电子式 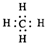 |
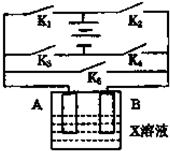 某课外活动小组准备用如图所示的装置进行实验,现有甲、乙、丙三位同学分别选择了如下电极材料和电解质溶液
某课外活动小组准备用如图所示的装置进行实验,现有甲、乙、丙三位同学分别选择了如下电极材料和电解质溶液| A电极 | B电极 | X溶液 | |
| 甲 | Cu | Zn | H2SO4 |
| 乙 | Pt | Pt | CuCl2 |
| 丙 | Fe | Cu | ? |
| A、甲同学在实验中将开关K5闭合,Zn电极上产生气泡 |
| B、乙同学打算闭合K3、K4做电解CuCl2溶液的实验 |
| C、乙同学用淀粉碘化钾试纸检验电解产生的氯气 |
| D、丙同学准备在Fe上镀Cu,选择了一种铜盐来配制电镀液,闭合的开关的组合是K2、K3 |
如图物质一定属于同系物的是( )
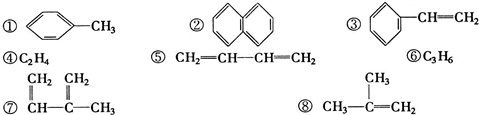

| A、①和②、④和⑥ |
| B、⑤和⑦、④和⑧ |
| C、④和⑥、⑤和⑦ |
| D、④和⑥、⑧ |