题目内容
16.下列有关说法正确的是( )| A. | 5.6 g铁与足量Cl2充分反应,转移电子数为0.2×6.02×1023 | |
| B. | 由PbO2+4HCl(浓)═PbCl2+Cl2↑+2H2O可确定氧化性:PbO2>Cl2 | |
| C. | 2Na2O2(s)+2CO2(g)═2Na2CO3(s)+O2(g)在常温下能自发进行,则该反应的△H>0 | |
| D. | 常温下,用蒸馏水不断稀释0.1 mol•L-1醋酸,溶液中c(H+)/c(CH3COOH)的值减小 |
分析 A.氯气具有强氧化性,与变价金属反应生成高价态的氯化物,铁与足量氯气反应生成氯化铁;
B.自发进行的氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性;
C.根据△G=△H-T•△S<0自发判断;
D.醋酸为弱酸,稀释过程中醋酸的电离程度增大,溶液中氢离子、醋酸根离子的物质的量增大,醋酸的物质的量减小,再结合溶液体积相同分析.
解答 解:A.5.6g铁为0.1mol,与足量氯气充分反应生成氯化铁,转移的电子数为0.3NA,即转移电子数为0.3×6.02×1023,故A错误;
B.PbO2+4HCl═PbCl2+Cl2↑+2H2O 中Pb元素化合价由+4价变为+2价、Cl元素化合价由-1价变为0价,所以 PbO2是氧化剂、Cl2是氧化产物,氧化性PbO2>Cl2,故B正确;
C.2Na2O2(s)+2CO2(g)═2Na2CO3(s)+O2(g),气体体积减小混乱度减小,△S<0,在常温下能自发进行,△G=△H-T•△S<0,则该反应的△H<0,故C错误;
D.稀释过程中氢离子的物质的量增大、醋酸的物质的量减小,由于在同一溶液中,溶液体积相同,则溶液中c(H+)/c(CH3COOH)的值增大,故D错误;
故选B.
点评 本题考查了氯气的性质、氧化性的比较、反应进行的方向判断、以及弱电解质的电离,掌握相关的知识是解答关键,试题培养了学生的灵活应用基础知识的能力,题目难度中等.

练习册系列答案
相关题目
6.下列变化属于放热反应的是( )
①碳与二氧化碳化合 ②生石灰与水反应生成熟石灰 ③Zn与稀硫酸反应
④浓硫酸溶于水 ⑤Ba(OH)2•8H2O与NH4Cl反应 ⑥甲烷与氧气的燃烧.
①碳与二氧化碳化合 ②生石灰与水反应生成熟石灰 ③Zn与稀硫酸反应
④浓硫酸溶于水 ⑤Ba(OH)2•8H2O与NH4Cl反应 ⑥甲烷与氧气的燃烧.
| A. | ①②④⑥ | B. | ①④⑤ | C. | ②③⑥ | D. | ②④⑥ |
7.已知反应X+Y=M+N为吸热反应,对这个反应的下列说法中正确的是( )
| A. | X的能量一定低于M的,Y的能量一定低于N的 | |
| B. | 因为该反应为吸热反应,故一定要加热反应才能进行 | |
| C. | 破坏反应物中的化学键所吸收的能量大于形成生成物中化学键所放出的能量 | |
| D. | 反应物X和Y的总能量一定大于生成物M和N的总能量 |
4.NO因污染空气而“臭名昭著”,而奇妙的作用也使期成为“明星分子”.如可用于制HNO3.肥料.炸药.促进血管扩张.促进免疫功能.增强记忆等.下列各组物质中,不能生成NO的是( )
| A. | Cu+HNO3(稀) | B. | N2+O2 | C. | NH4Cl+O2 | D. | NO2+H2O |
11.电解质溶液的电导率越大,导电能力越强.用0.100mol•L-1的NaOH溶液滴定10.00mL浓度均为0.100mol•L-1 的盐酸和CH3COOH溶液.利用传感器测得滴定过程中溶液的电导率如图所示.下列说法不正确的是( )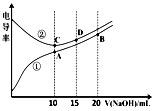

| A. | 曲线①代表滴定CH3COOH溶液的曲线 | |
| B. | A点溶液中:c(CH3COO-)+c(OH-)-c(H+)=0.05mol•L-1 | |
| C. | 在相同温度下,A、B、C三点溶液中水电离的c(H+):B<A=C | |
| D. | B点溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
1.以下反应均可生成O2.下列有关说法正确的是( )
①二氧化碳分解生成氧气:2CO2(g)═2CO(g)+O2(g);△H1=566kJ•mol-1
②过氧化氢分解生成氧气:2H2O2(l)═2H2O(l)+O2(g);△H2=-196.4kJ•mol-1
③光照条件下,催化分解水蒸气生成氧气:2H2O(g)═2H2(g)+O2(g);△H3=483.6kJ•mol-1.
①二氧化碳分解生成氧气:2CO2(g)═2CO(g)+O2(g);△H1=566kJ•mol-1
②过氧化氢分解生成氧气:2H2O2(l)═2H2O(l)+O2(g);△H2=-196.4kJ•mol-1
③光照条件下,催化分解水蒸气生成氧气:2H2O(g)═2H2(g)+O2(g);△H3=483.6kJ•mol-1.
| A. | 反应①使用催化剂,能降低该反应的活化能 | |
| B. | 反应②为吸热反应 | |
| C. | 反应③将化学能转化为光能 | |
| D. | 反应CO(g)+H2O(g)═CO2(g)+H2(g);△H=-82.4 kJ•mol-1 |
8.下列不属于碱的是( )
| A. | 烧碱 | B. | 纯碱 | C. | 熟石灰 | D. | 一水合氨 |
5.下列有关元素性质的递变规律不正确的是( )
| A. | Na、Mg、Al的金属性依次减弱 | B. | H2S、H2O、HF的稳定性依次减弱 | ||
| C. | Cl-、Br-、I- 还原性依次增强 | D. | Na、K、Rb的原子半径依次增大 |
10.有主族元素形成的3种离子Xn+,Ym-,Zm+,已知m>n,Xn+比Zm+多一个电子层,Z与Y同周期,三种原子的M层电子数均为偶数,下列推断不正确的是( )
| A. | 原子半径X>Y>Z | |
| B. | 离子半径Ym->Xn+>Zm+ | |
| C. | 三种元素最高价氧化物对应水化物碱性依次减弱,酸性依次增强的顺序是X,Z,Y | |
| D. | Y在自然界中没有游离态,可形成原子晶体 |