题目内容
铁及其合金在生产、生活中应用广泛,下列说法中正确的是( )
| A、生铁中含有碳,抗腐蚀能力比纯铁强 |
| B、铁与盐溶液所发生的反应都是置换反应 |
| C、铁与稀硫酸反应,铁与浓硫酸不能反应 |
| D、工业上可以用铝热反应的方法制取少量的铁 |
考点:铁的化学性质
专题:元素及其化合物
分析:A.构成原电池负极的金属加速被腐蚀;
B.铁和盐溶液发生的反应可能是化合反应;
C.铁和浓硫酸发生钝化现象;
D.铝的还原性大于铁,工业上可以采用铝热反应制备少量铁.
B.铁和盐溶液发生的反应可能是化合反应;
C.铁和浓硫酸发生钝化现象;
D.铝的还原性大于铁,工业上可以采用铝热反应制备少量铁.
解答:
解:A.Fe、C和电解质溶液构成原电池,Fe易失电子作负极加速被腐蚀,纯铁和电解质溶液发生化学腐蚀,所以生铁抗腐蚀性小于纯铁,故A错误;
B.铁和盐溶液发生的反应可能是化合反应,如Fe+2FeCl3=3FeCl2,故B错误;
C.铁和浓硫酸发生氧化还原反应生成一层致密的氧化物薄膜而阻止进一步被氧化,该现象为钝化现象,故C错误;
D.铝的还原性大于铁,工业上可以采用铝热反应制备少量铁,常常用于铁轨焊接,故D正确;
故选D.
B.铁和盐溶液发生的反应可能是化合反应,如Fe+2FeCl3=3FeCl2,故B错误;
C.铁和浓硫酸发生氧化还原反应生成一层致密的氧化物薄膜而阻止进一步被氧化,该现象为钝化现象,故C错误;
D.铝的还原性大于铁,工业上可以采用铝热反应制备少量铁,常常用于铁轨焊接,故D正确;
故选D.
点评:本题侧重考查元素化合物知识,明确铁的性质是解本题关键,注意铁和浓硫酸发生钝化现象时实际上发生化学反应,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列表达方式正确的是( )
| A、乙烯的结构简式CH2CH2 |
B、基态氧原子L层电子排布图: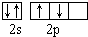 |
C、甲基的电子式 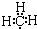 |
| D、HClO的结构式:H-Cl-O |
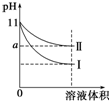 某温度下,pH=11的氨水和NaOH溶液分别加水稀释100倍,溶液的pH随溶液体积变化的曲线如图所示.据图判断错误的是( )
某温度下,pH=11的氨水和NaOH溶液分别加水稀释100倍,溶液的pH随溶液体积变化的曲线如图所示.据图判断错误的是( )| A、a的数值一定大于9 |
| B、Ⅱ为氨水稀释时溶液的pH变化曲线 |
| C、稀释后氨水中水的电离程度比NaOH溶液中水的电离程度大 |
| D、完全中和相同体积的两溶液时,消耗相同浓度的稀硫酸的体积V(NaOH)<V(氨水) |
下列关于“纯碱”的分类正确的是( )
| A、酸 | B、碱 | C、盐 | D、电解质 |
有一无色混合物的水溶液,只能含有一下离子中的若干种;H+、K+、NH4+、Mg2+、Fe3+、Cl-、CO32-、SO42-,现取三份100ml溶液进行如下实验:根据上述实验,一下推测正确的是( )
(1)第一份加入足量AgNO3溶液有沉淀产生;
(2)第二份加入足量NaOH溶液加热后,收集到气体0.04mol;
(3)第三份加入足量BaCl2溶液后,得到沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g.
(1)第一份加入足量AgNO3溶液有沉淀产生;
(2)第二份加入足量NaOH溶液加热后,收集到气体0.04mol;
(3)第三份加入足量BaCl2溶液后,得到沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g.
| A、K+一定存在 |
| B、100ml溶液中含0.01molCO32- |
| C、Cl-一定存在 |
| D、Fe3+一定不存在,Mg2+可能存在 |
将反应4(NH4)2SO4→N2↑+6NH3↑+3SO2↑+SO3↑+7H2O的产物气体通入BaCl2溶液,下列判断正确的是( )
| A、无沉淀生成 |
| B、得到的沉淀是BaSO4和BaSO3组成的混合物 |
| C、得到的沉淀是纯净物 |
| D、肯定没有BaSO3生成 |
 烧杯中装有100mLH2SO4和Na2SO4的混合液,其浓度分别为0.16mol/L和2mol/L,欲使其浓度分别变为1.6mol/L和0.2mol/L,在只有蒸馏水和18mol/L浓H2SO4以及必要仪器的条件下,完成任务:
烧杯中装有100mLH2SO4和Na2SO4的混合液,其浓度分别为0.16mol/L和2mol/L,欲使其浓度分别变为1.6mol/L和0.2mol/L,在只有蒸馏水和18mol/L浓H2SO4以及必要仪器的条件下,完成任务: