题目内容
SO2是硫酸工业尾气的主要成分.实验室中,拟用如图所示流程,测定标准状况下,体积为VL的硫酸工业尾气中SO2的含量:

(1)步骤①中加入H2O2溶液时发生反应的离子方程式为 ,1mol H2O2参加反应,转移的电子数为 .
(2)步骤③的操作依次是: 、 、 、称重.
(3)该VL尾气中SO2的体积分数为 (用含有V、m的代数式表示).

(1)步骤①中加入H2O2溶液时发生反应的离子方程式为
(2)步骤③的操作依次是:
(3)该VL尾气中SO2的体积分数为
考点:探究物质的组成或测量物质的含量
专题:
分析:(1)步骤①中加入H2O2溶液,过氧化氢与SO2反应生成H2SO4;根据元素化合价的变化分析计算转移的电子数;
(2)步骤③的操作是从溶液中分离出沉淀硫酸钡,操作步骤是过滤、洗涤、干燥、称重;
(3)mg是硫酸钡的质量,计算硫酸钡的物质的量,根据硫元素守恒计算二氧化硫的体积,进而计算二氧化硫的体积分数.
(2)步骤③的操作是从溶液中分离出沉淀硫酸钡,操作步骤是过滤、洗涤、干燥、称重;
(3)mg是硫酸钡的质量,计算硫酸钡的物质的量,根据硫元素守恒计算二氧化硫的体积,进而计算二氧化硫的体积分数.
解答:
解:(1)步骤①中加入H2O2溶液,过氧化氢具有氧化性,二氧化硫具有还原性被氧化为硫酸,发生反应的离子方程式为H2O2+SO2=2H+++SO42-,1mol过氧化氢反应转移电子物质的量为2mol,转移的电子数为2×6.02×1023=1.204×1024;
故答案为:H2O2+SO2=2H+++SO42-,1.204×1024;
(2)步骤③的操作是从溶液中分离出沉淀硫酸钡,操作步骤是过滤、洗涤、干燥、称重;
故答案为:过滤、洗涤、干燥;
(3)mg是硫酸钡的质量,硫酸钡的物质的量为
=
mol,根据硫元素守恒可知二氧化硫的体积为
mol×22.4L/mol=
L,故尾气中二氧化硫的体积分数=
=
×100%;
故答案:
×100%.
故答案为:H2O2+SO2=2H+++SO42-,1.204×1024;
(2)步骤③的操作是从溶液中分离出沉淀硫酸钡,操作步骤是过滤、洗涤、干燥、称重;
故答案为:过滤、洗涤、干燥;
(3)mg是硫酸钡的质量,硫酸钡的物质的量为
| mg |
| 233g/mol |
| m |
| 233 |
| m |
| 233 |
| 22.4m |
| 233 |
| ||
| VL |
| m×22.4 |
| 233V |
故答案:
| m×22.4 |
| 233V |
点评:本题考查学生对实验原理与实验操作的理解、实验方案设计、元素化合物性质、化学计算等,难度中等,清楚实验原理是解题的关键,需要学生具备扎实的基础知识与综合运用知识分析问题、解决问题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列各物质既能发生消去反应生成相应的烯烃,又能氧化成相应的醛的是( )
| A、CH3OH |
| B、(CH3)3COH |
| C、CH3CHOHCH3 |
| D、CH3CH2CH2OH |
在无色溶液中,下列离子能大量共存的是( )
| A、Cu2+、SO42-、Na+、Cl- |
| B、Na+、CO32-、H+、K+ Ba2+ |
| C、Ag+、NO3-、K+、Cl- |
| D、Mg2+、H+、SO42-、NO3- |
我国继“食盐加碘”后,又启动了“酱油加铁”工程.“酱油加铁”的意义是( )
(1)补充人体需要的铁元素 (2)预防缺铁性贫血病 (3)改善酱油的味道
(4)增加黑色素 (5)减少厨房污染物 (6)提高人们的健康水平.
(1)补充人体需要的铁元素 (2)预防缺铁性贫血病 (3)改善酱油的味道
(4)增加黑色素 (5)减少厨房污染物 (6)提高人们的健康水平.
| A、(1)(2)(3) |
| B、(4)(5)(6) |
| C、(3)(4)(5) |
| D、(1)(2)(6) |
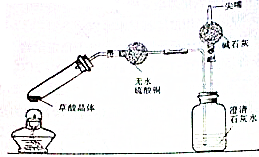 有资料表明:乙二酸(HOOC-COOH,可简写为H2C2O4)俗称草酸,是一种白色固体,易溶于水,其熔点为101.5℃,在157℃升华,其钙盐不溶于水.某校化学研究性学习小组为探究草酸受热分解的产物,甲同学设计如图所示的装置.装置中试管口向上倾斜,其原因是
有资料表明:乙二酸(HOOC-COOH,可简写为H2C2O4)俗称草酸,是一种白色固体,易溶于水,其熔点为101.5℃,在157℃升华,其钙盐不溶于水.某校化学研究性学习小组为探究草酸受热分解的产物,甲同学设计如图所示的装置.装置中试管口向上倾斜,其原因是