题目内容
3.一定温度下的密闭容器中有反应2SO2(g)+O2 (g)?2SO3 (g),下列叙述能说明该反应达到平衡状态的是( )| A. | 正、逆反应速率相等均为零 | |
| B. | 反应物和生成物的浓度保持一定 | |
| C. | SO2、O2、SO3分子数目之比为2:1:2 | |
| D. | 单位时间内消耗a mol SO2,同时生成a mol SO3 |
分析 可逆反应2SO2(g)+O2 (g)?2SO3 (g)为气体体积缩小的反应,该反应达到平衡状态时,正反应速率与逆反应速率相等,各组分的浓度、百分含量不再变化,据此进行解答.
解答 解:A.达到平衡状态时,正逆反应速率相等,但不等于0,故A错误;
B.反应物和生成物的浓度保持一定,表明正逆反应速率相等,该反应达到平衡状态,故B正确;
C.SO2、O2、SO3分子数目之比为2:1:2,无法判断正逆反应速率是否相等,则无法判断平衡状态,故C错误;
D.单位时间内消耗a mol SO2,同时生成a mol SO3,表示的都是正反应速率,无法判断正逆反应速率是否相等,故D错误;
故选B.
点评 本题考查了化学平衡状态的判断,题目难度不大,明确化学平衡状态的特征为解答关键,注意可逆反应达到平衡状态时正逆反应速率相等,但不等于0,试题侧重基础知识的考查,培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
11.以下各组物质既不是同系物也不是同分异构体的是( )
| A. | CH4和C10 H22 | B. | 1-己烯和环己烷 | C. | C2H4和1-丁烯 | D. | 乙二醇和丙三醇 |
18.短周期元素X、Y、Z、W原子序数依次增大,它们原子的最外层电子数之和为14.X与Z同主族,Y与W同主族,且X的原子半径小于Y.下列叙述正确的是( )
| A. | 原子半径:Y<Z<W | |
| B. | Z在化合物中呈+1价 | |
| C. | Y与W可形成离子化合物 | |
| D. | W的单质能在Y的单质中燃烧生成WY3 |
8.如图为周期表中短周期的一部分,若X原子最外层电子数比次外层电子数少3,则下列说法正确的是( )
| R | ||
| X | Y | Z |
| A. | X的氢化物比R的氢化物稳定 | |
| B. | 原子半径大小顺序是Z>Y>X>R | |
| C. | Z的单质能与Y的某些化合物发生置换反应 | |
| D. | X、Y、Z氢化物的稳定性:XH3>H2Y>HZ |
13.某溶液可能含有K+、Na+、SO42-、AlO2-、NO3-、I-、Fe2+、Al3+、SiO32-.现进行如下实验:由此可知原溶液中( )
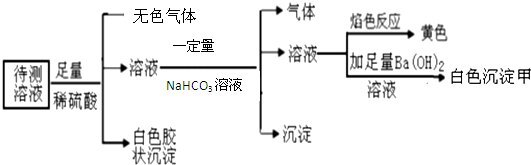

| A. | 一定含有Na+,可能存在K+ | |
| B. | 至少存在4种离子 | |
| C. | 无色气体是NO气体 | |
| D. | 白色沉淀甲中一定含有BaSO4和BaCO3 |