题目内容
SO2、SO3、CO、Fe2O3是四种常见的氧化物,它们能发生多个反应.分别写出符合下列要求的化学方程式.
(1)Fe2O3和CO在高温下反应 ;
(2)能够说明Fe2O3是碱性氧化物的反应 (只写一个);
(3)SO2和足量KOH溶液反应 ;
(4)已知SO3是一种能和水反应的酸性氧化物,SO3能和NaOH溶液反应 .
(1)Fe2O3和CO在高温下反应
(2)能够说明Fe2O3是碱性氧化物的反应
(3)SO2和足量KOH溶液反应
(4)已知SO3是一种能和水反应的酸性氧化物,SO3能和NaOH溶液反应
考点:二氧化硫的化学性质,铁的氧化物和氢氧化物
专题:元素及其化合物
分析:(1)Fe2O3和CO在高温下发生氧化还原反应生成Fe和CO2;
(2)Fe2O3可与酸反应生成盐和水;
(3)SO2和足量KOH溶液反应生成K2SO3和水;
(4)SO3和足量KOH溶液反应生成K2SO4和水.
(2)Fe2O3可与酸反应生成盐和水;
(3)SO2和足量KOH溶液反应生成K2SO3和水;
(4)SO3和足量KOH溶液反应生成K2SO4和水.
解答:
解:(1)Fe2O3和CO在高温下发生氧化还原反应生成Fe和CO2,反应的方程式为Fe2O3+3CO
2Fe+3CO2,故答案为:Fe2O3+3CO
2Fe+3CO2;
(2))Fe2O3可与酸反应生成盐和水,反应的方程式为Fe2O3+3HCl=2FeCl3+3H2O,故答案为:Fe2O3+3HCl=2FeCl3+3H2O;
(3)SO2和足量KOH溶液反应生成K2SO3和水,反应的方程式为SO2+2KOH=K2SO3+H2O,故答案为:SO2+2KOH=K2SO3+H2O;
(4)SO3和足量KOH溶液反应生成K2SO4和水,反应的方程式为SO3+2NaOH=Na2SO4+H2O,故答案为:SO3+2NaOH=Na2SO4+H2O.
| ||
| ||
(2))Fe2O3可与酸反应生成盐和水,反应的方程式为Fe2O3+3HCl=2FeCl3+3H2O,故答案为:Fe2O3+3HCl=2FeCl3+3H2O;
(3)SO2和足量KOH溶液反应生成K2SO3和水,反应的方程式为SO2+2KOH=K2SO3+H2O,故答案为:SO2+2KOH=K2SO3+H2O;
(4)SO3和足量KOH溶液反应生成K2SO4和水,反应的方程式为SO3+2NaOH=Na2SO4+H2O,故答案为:SO3+2NaOH=Na2SO4+H2O.
点评:本题综合考查元素化合物知识,为高频考点,侧重于元素化合物知识的综合理解和运用的考查,注意相关物质的性质,把握方程式的书写,难度不大.

练习册系列答案
相关题目
一定条件下发生反应 2KClO3+I2═2KIO3+Cl2↑,由此可推断,下列相应结论不正确的是( )
| A、I2具有氧化性 |
| B、该反应属于氧化还原反应 |
| C、氧化剂是KClO3 |
| D、I2是还原剂 |
下列说法中正确的是( )
| A、淀粉、纤维素和油脂都属于天然高分子化合物 |
| B、合成纤维、人造纤维及碳纤维都属于有机高分子材料 |
| C、蔗糖、淀粉、油脂及其水解产物均为非电解质 |
| D、石油是混合物,其分馏产品汽油也为混合物 |
下列情况会对人体健康造成较大危害的是( )
| A、自来水中通入少量Cl2进行消毒杀菌 |
| B、用SO2漂白食品 |
| C、用食醋清洗热水瓶胆内壁附着的水垢 |
| D、用小苏打发酵面团制作馒头 |
室温下,将0.4mol/L HA溶液和0.2mol/LNaOH溶液等体积混合(忽略混合时溶液体积的变化)测得混合溶液的pH=5,则下列说法(或关系式)正确的是( )
| A、混合溶液中由水电离出的c(H+)=1×10-5mol/L |
| B、c(A-)+c(HA)=2c(Na+)=0.4 mol/L |
| C、c(HA)>c(A-)>c(Na+)>c(H+)>c (OH-) |
| D、c(A-)-c(HA)=2c(H+)-2 c(OH-) |
下列化学反应的速率,一定是前者大于后者的( )
| A、一定温度下,相同氢离子浓度、相同体积的盐酸与硫酸分别与大小相同的锌片反应,产生气泡的快慢 | ||||
B、反应A+B
| ||||
| C、相同温度下,与同浓度盐酸反应的锌粉和铁粉产生氢气的速率 | ||||
| D、相同温度下,颗粒大小相同的生铁分别在水和饱和食盐水中的腐蚀 |
根据反应式:(1)2Fe3++2I-═2Fe2++I2;(2)Br2+2Fe2+═2Br-+2Fe3+,可判断离子的还原性从强到弱的顺序是( )
| A、I->Fe2+>Br- |
| B、Br->Fe2+>I- |
| C、Br->I->Fe2+ |
| D、Fe2+>I->Br- |

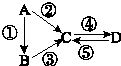 A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系:
A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系: