题目内容
如图为元素周期表的一部分,已知A、B、C、D、E,5个原子共有85个电子,E原子核外有4个电子层,则B元素是( )
| A | ||
| C | B | D |
| E |
| A、P | B、Mg | C、Cl | D、Si |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:E原子核外有四个电子层,处于第四周期,则A处于第二周期,C、B、D处于第四周期,A,B,C,D,E五种元素原子核外共有85个电子,则元素所处的周期处于过渡元素之后,令B的核外电子数为x,则C核外电子数为x-1,D核外电子数为x+1,A核外电子数为x-8,E核外电子数为x+18,列方程计算x的值,进而确定各元素解答.
解答:
解:E原子核外有四个电子层,处于第四周期,则A处于第二周期,C、B、D处于第四周期,A,B,C,D,E五种元素原子核外共有85个电子,则元素所处的周期处于过渡元素之后,令B的核外电子数为x,则C核外电子数为x-1,D核外电子数为x+1,A核外电子数为x-8,E核外电子数为x+18,则:x-1+x+x+1+x-8+x+18=85,解得x=15,故B为P元素,故选A.
点评:本题考查元素推断,难度不大,注意理解掌握同主族元素原子序数关系,判断元素所处的周期处于过渡元素之后是关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
a L CO和O2的混合气体,点燃后得到b L气体(前后条件相同),则混合气体中CO的体积可能是下列组合中的( )
①b ②
a ③a-b ④a+b ⑤2(a-b)
①b ②
| 2 |
| 3 |
| A、①②③ | B、②④⑤ |
| C、①②④ | D、①②⑤ |
下列说法正确的是( )
| A、Na2CO3溶液中加入少量Ca(OH)2 固体,CO32-水解程度减小,溶液的pH减小 | ||
| B、25℃时,用醋酸溶液滴定等浓度NaOH溶液至pH=7,V(醋酸)<V(NaOH) | ||
| C、向NaAlO2溶液中滴加NaHCO3溶液,有沉淀和气体生成 | ||
D、CH3COOH 溶液加水稀释后,溶液中
|
下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( ) 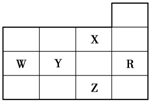

| A、其气态氢化物的稳定性是X>Y>W>Z |
| B、其最高价氧化物对应的水化物的酸性:Y>W |
| C、电负性、第一电离能的大小顺序都是X>Y>W |
| D、Y、Z的阴离子电子层结构都与R原子的相同 |
某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路.课外活动小组为确认生产后的废液的组成,进行如下实验:(1)取10mL废液加入足量的AgNO3溶液,生成沉淀8.61g.(2)另取10mL废液放入铜片充分反应,铜片质量减少了0.256g.下列关于原废液组成的判断正确的是( )
| A、c(Cu2+)=c(Fe2+) |
| B、c(Fe2+)+c(Cu2+)+c(Fe 3+)=c(Cl-) |
| C、c(Cu2+)+c(Fe3+)=1.4 mol/L |
| D、c(Fe3+)+c(Fe2+)=6 mol/L |
下列化学用语错误的是( )
A、过氧化钡的电子式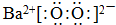 | ||
B、钠-23的原子符号
| ||
| C、次氯酸的结构式 H-Cl-O | ||
| D、锰酸根MnO42- |
下列能达到实验目的是( )
A、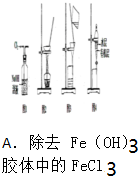 除去Fe(OH)3胶体中的FeCl3 |
B、 干燥、收集氨气,并吸收多余的氨气 |
C、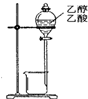 分离乙醇、乙酸 |
D、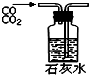 除去杂质气体CO2 |
下列说法正确的是( )
| A、摩尔是物质的质量单位 |
| B、物质的量是国际单位制中七个基本单位之一 |
| C、阿伏加德罗常数是12 g 12C中含有的碳原子数目 |
| D、标准状况下,1 mol H2O所占的体积为22.4L |
下列各组物理量中,都不随取水量的变化而变化的是( )
| A、水的沸点;蒸发水所需热量 |
| B、水的密度;水中通入足量CO2后溶液的pH |
| C、水的体积;水的质量 |
| D、水的物质的量;水的摩尔质量 |