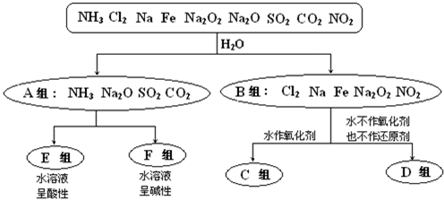
题目内容
14.下列有关有机物分离提纯或除杂的方法正确的是( )| A. | 溴苯中混有溴,加入KI溶液,振荡,用汽油萃取出I2 | |
| B. | 除去乙醇中的微量水可加入金属钠,使其完全反应 | |
| C. | 乙酸乙酯中有乙酸杂质,可以加入氢氧化钠溶液,充分反应后静置分液 | |
| D. | 乙烯中混有CO2和SO2,将其通过盛有NaOH溶液的洗气瓶,再干燥 |
分析 A.碘、汽油与苯混溶;
B.二者都与钠反应;
C.二者都与氢氧化钠反应;
D.二氧化碳、二氧化硫都与氢氧化钠溶液反应.
解答 解:A.碘、汽油与苯混溶,不能得到纯净的苯,应加入氢氧化钠溶液,然后分液,故A错误;
B.二者都与钠反应,可加入氧化钙,然后蒸馏,故B错误;
C.二者都与氢氧化钠反应,因乙酸乙酯不溶于饱和碳酸钠溶液,乙酸与碳酸钠溶液反应,可用饱和碳酸钠溶液除杂,故C错误;
D.二氧化碳、二氧化硫都与氢氧化钠溶液反应,可达到除杂的目的,故D正确.
故选D.
点评 本题考查物质的分离、提纯,为高考常见题型和高频考点,侧重于学生的分析能力和实验能力的考查,本题主要在除杂时不能引入新杂质,更不能影响被提纯的物质,难度不大.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案
相关题目
4. 某实验小组以H2O2分解为例,研究浓度、催化剂、溶液的酸碱性①对反应速率的影响.在常温下按照如表方案完成实验.
某实验小组以H2O2分解为例,研究浓度、催化剂、溶液的酸碱性①对反应速率的影响.在常温下按照如表方案完成实验.
(1)催化剂能加快化学反应速率的原因是降低了反应的活化能.
(2)实验①和②的目的是探究浓度对反应速率的影响.
实验时由于没有观察到明显现象而无法得出结论.资料显示,通常条件下H2O2稳定,不易分解.为了达到实验目的,你对原实验方案的改进是向反应物中加入等量同种催化剂(或将盛有反应物的试管放入同一热水浴中).
(3)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图所示.分析图示能够得出的实验结论是碱性环境能增大H2O2分解的速率,酸性环境能减小H2O2分解的速率.
 某实验小组以H2O2分解为例,研究浓度、催化剂、溶液的酸碱性①对反应速率的影响.在常温下按照如表方案完成实验.
某实验小组以H2O2分解为例,研究浓度、催化剂、溶液的酸碱性①对反应速率的影响.在常温下按照如表方案完成实验.| 编号 | 反应物 | 催化剂 |
| ① | 10mL 2%H2O2溶液 | 无 |
| ② | 10mL 5% H2O2溶液 | 无 |
| ③ | 10mL 5%H2O2溶液 | 1mL 0.1mol•L-1FeCl3溶液 |
| ④ | 10mL 5% 5H2O2溶液+少量HCl溶液 | 1mL 0.1mol•L-1FeCl3溶液 |
| ⑤ | 10mL 5%H2O2溶液+少量NaOH溶液 | 1mL 0.1mol•L-1FeCl3溶液 |
(2)实验①和②的目的是探究浓度对反应速率的影响.
实验时由于没有观察到明显现象而无法得出结论.资料显示,通常条件下H2O2稳定,不易分解.为了达到实验目的,你对原实验方案的改进是向反应物中加入等量同种催化剂(或将盛有反应物的试管放入同一热水浴中).
(3)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图所示.分析图示能够得出的实验结论是碱性环境能增大H2O2分解的速率,酸性环境能减小H2O2分解的速率.
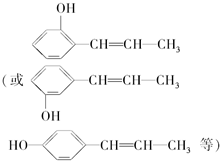
5.6月26日是国际禁毒日,据公安部通报,目前冰毒、摇头丸、氯胺酮等新型毒品在我国有较大传播范围,吸、贩新型毒品问题十分突出.已知下列四种毒品的结构简式:
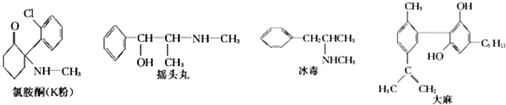
下列说法不正确的是( )

下列说法不正确的是( )
| A. | 冰毒能与盐酸反应 | |
| B. | 摇头丸具有两性 | |
| C. | 1molK粉最多可以与4molH2发生加成反应 | |
| D. | 适当条件下,1mol大麻最多可与3mol Br2发生反应 |
2.下列电离方程式中,书写正确的是( )
| A. | Ba(OH)2?Ba2++2 OH- | B. | H3PO4?3 H++PO43- | ||
| C. | NaHCO3═Na++H++CO3 2- | D. | HClO?H++ClO- |
19.下列化学用语表述正确的是( )
| A. | HC1的电子式: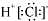 | B. | 乙烯分子的结构简式:CH2CH2 | ||
| C. | S2-的原子结构示意图: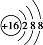 | D. | H2O2的电子式: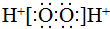 |
6.如图是元素周期表的轮廓图,通常用于制造农药的元素所在的区域是( )
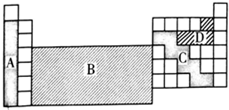

| A. | A | B. | B | C. | C | D. | D |
3.按要求填写表:
| 分子 | a | 孤对电子数 | δ键数 | VSEPR模型 | 空间构型 |
| CO2 | 4 | 0 | 2 | 直线形 | 直线形 |
| SO2 | 6 | 1 | 2 | 四面体 | V形 |
| NH3 | 5 | 1 | 3 | 四面体 | 三角锥形 |
| CCl4 | 4 | 0 | 4 | 正四面体 | 正四面体 |

 .
. .
.