题目内容
17.两种气态烃的混合物共0.1mol,完全燃烧后得到3.36L CO2(标准状况)和3.6g H2O,下列说法正确的是( )| A. | 一定有乙烯 | B. | 一定有甲烷 | ||
| C. | 一定没有乙烯 | D. | 可能是甲烷和丁烯的混合物 |
分析 标况下3.36L二氧化碳的物质的量为:n(CO2)=$\frac{3.36L}{22.4L/mol}$=0.15mol,3.6g水的物质的量为:n(H2O)=$\frac{3.6g}{18g/mol}$=0.2mol,则混合的平均化学式为,C1.5H4,由于是混合物,则肯定含有C原子数小于1.5的烃,即一定含有甲烷,因甲烷中含有4个氢原子,则另一种烃也含有4个氢原子,以此进行解答.
解答 解:标况下3.36L二氧化碳的物质的量为:n(CO2)=$\frac{3.36L}{22.4L/mol}$=0.15mol,3.6g水的物质的量为:n(H2O)=$\frac{3.6g}{18g/mol}$=0.2mol,
1mol混合气体完全燃烧生成1.5mol二氧化碳、2mol水,则混合的平均化学式为:C1.5H4,
由于两种气态烃的混合物,则一定含有C原子数小于1.5的烃,所以一定含有甲烷,
又由于甲烷中含4个氢原子,则另一种烃也含有4个氢原子,
根据以上分析可知,混合气体中一定含有甲烷,所以B正确;可能含有乙烯、丙炔,一定不含丁烯,所以A、C、D错误,
故选B.
点评 本题考查了有机物分子式的计算,题目难度中等,注意掌握利用平均分子组成判断烃的组成的方法,明确确定有机物组成时常用方法:平均碳法、平均氢法、平均碳氢分子式法、平均式量法等.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案
相关题目
7.下列有关化学反应现象或化学原理的解释不正确的是( )
| 选项 | 现象或反应 | 原理解释 |
| A | 2CO=2C+O2在任何条件下均不能自发进行 | 该反应△H>0,△S>0 |
| B | 铝箔在酒精灯火焰上加热融化但不滴落 | Al2O3熔点高于Al单质 |
| C | 蒸馏时,温度计的球泡应靠近蒸馏烧瓶支管口处 | 此位置指示的是被蒸馏物质的沸点 |
| D | KI淀粉溶液中滴入氯水变蓝,再通入SO2,蓝色褪色 | SO2具有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
5.氨催化氧化法制硝酸的原理为4NH3(g)+5O2(g)$?_{△}^{Pt}$4NO(g)+6H2O(g).在浓氨水中通入空气,将赤热铂
丝插入氨水中引发反应后铂丝保持红热状态至反应停止.下列说法正确的是( )
丝插入氨水中引发反应后铂丝保持红热状态至反应停止.下列说法正确的是( )
| A. | 上述反应在较高温度下才能自发进行 | |
| B. | 该反应的正反应活化能小于逆反应活化能 | |
| C. | 该反应中,断裂化学键的总键能大于形成化学键的总键能 | |
| D. | 若NH3和O2的混合气发生上述反应,气体通入足量水中,剩余气体一定是O2 |
12.下列物质间的反应不属于离子反应的是( )
| A. | CO+O2 | B. | NaCl+AgNO3 | C. | CaCO3+HCl | D. | CuO+H2 |
2.下列装置中,电流表指针不能发生偏转的是( )
| A. | 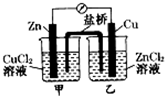 | B. | 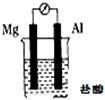 | ||
| C. | 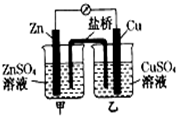 | D. | 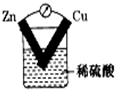 |
9.现有四种元素的基态原子的电子排布式如下:①1s22s22p63s23p1;②1s22s22p63s23p3;③1s22s22p5.则下列有关比较中正确的是( )
| A. | 第一电离能:③>②>① | B. | 原子半径:③>②>① | ||
| C. | 电负性:③<②<① | D. | 最高正化合价:③>②>① |
7.下列有关合成氨工业的叙述,可用勒夏特列原理来解释的是( )
| A. | 使用铁触媒,使N2和H2混合气体有利于合成氨 | |
| B. | 高压比常压条件更有利于合成氨的反应 | |
| C. | 700K左右比室温更有利于合成氨的反应 | |
| D. | 合成氨时采用循环操作,可提高原料的利用率 |