题目内容
19.下列变化过程,属于放热反应的是( )①Ba(OH)2•8H2O 与NH4Cl反应 ②酸碱中和 ③浓硫酸稀释 ④固体NaOH溶于水 ⑤硫在空气或氧气中燃烧.
| A. | ②③④⑤ | B. | ②③④ | C. | ②⑤ | D. | ①③⑤ |
分析 常见的放热反应有:所有的物质燃烧;所有金属与酸或与水;所有中和反应;绝大多数化合反应;铝热反应;
常见的吸热反应有:绝大数分解反应;个别的化合反应(如C和CO2);工业制水煤气;碳、一氧化碳、氢气还原金属氧化物;某些复分解(如铵盐和强碱).据此分析.
解答 解:①Ba(OH)2•8H2O 与NH4Cl反应是典型的吸热反应,故错误;
②酸碱中和是放热反应,故正确;
③浓硫酸稀释是放热的物理过程,不是化学反应,故错误;
④固体NaOH溶于水是放热的物理过程,不是化学反应,故错误;
⑤所有的燃烧均为放热反应,故硫在空气或氧气中燃烧是放热反应,故正确.
故选C.
点评 本题考查化学反应中能量变化,题目难度不大,掌握常见的放热反应和吸热反应是解题的关键.

练习册系列答案
相关题目
9.下列图示箭头方向表示与某种常见试剂在通常条件下(不含电解)发生转化,其中6步转化均能一步实现的一组物质是( )
| 选项 | W | X | Y | Z | 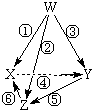 |
| A | N2 | NH3 | NO | NO2 | |
| B | Na | Na2O2 | NaOH | Na2CO3 | |
| C | Cu | CuSO4 | CuCl2 | Cu(OH)2 | |
| D | Al | Al2(SO4)3 | AlCl3 | NaAlO2 |
| A. | N2 NH3 NO NO2 | B. | Na Na2O2 NaOH Na2CO3 | ||
| C. | Cu CuSO4 CuCl2 Cu(OH)2 | D. | Al Al2(SO4)3 AlCl3 NaAlO2 |
10.下列离子方程式书写正确的是( )
| A. | 碳酸钙与盐酸反应:CO32-+2H+═CO2↑+H2O | |
| B. | 硫酸氢钠溶液中加入足量烧碱溶液:HSO4-+OH-═SO42-+H2O | |
| C. | Ba(OH)2与H2SO4反应到恰好沉淀完全:Ba2++OH-+SO42-+H+═BaSO4↓+H2O | |
| D. | 向澄清的石灰水中滴入少量碳酸氢钠溶液:Ca2++OH-+HCO3-═CaCO3↓+H2O |
7.下列有关氧化还原反应的说法正确的是( )
| A. | 一定有电子得失或偏移 | B. | 氧化反应一定先于还原反应 | ||
| C. | 氧化剂发生氧化反应 | D. | 其实质是元素化合价发生变化 |
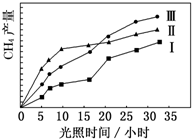 利用光能和光催化剂,可将 CO2 和 H2O(g)转化为 CH4 和 O2.紫外光照射时,在不同催化剂(Ⅰ,Ⅱ,Ⅲ)作用下,CH4产量随光照时间的变化如图所示.
利用光能和光催化剂,可将 CO2 和 H2O(g)转化为 CH4 和 O2.紫外光照射时,在不同催化剂(Ⅰ,Ⅱ,Ⅲ)作用下,CH4产量随光照时间的变化如图所示.