题目内容
9.化学使人类生活得更美好的一门自然科学.下列说法正确的是( )| A. | 豆浆富含蛋白质,煮沸后蛋白质变成了氨基酸 | |
| B. | 浓硫酸可刻蚀石英制艺术品 | |
| C. | 氢氧化铝可作胃酸的中和剂 | |
| D. | 装饰材料中释放的甲醛、苯不会造成污染 |
分析 A.蛋白质水解可生成氨基酸;
B.浓硫酸与二氧化硅不反应;
C.氢氧化铝为难溶物,能够中和胃酸中的盐酸;
D.甲醛、苯对人体有害,为环境污染物.
解答 解:A.蛋白质在解热条件下变性,在催化剂条件下水解可生成氨基酸,故A错误;
B.浓硫酸与二氧化硅不反应,应用氢氟酸,故B错误;
C.氢氧化铝能够与胃酸中的盐酸反应,能够作胃酸的中和剂,故C正确;
D.甲醛、苯常用作装饰材料,对人体有害,可致癌,为环境污染物,故D错误.
故选C.
点评 本题综合考查有机物的结构、性质以及应用,为高考常见题型,侧重于化学与生活、生产的考查,注意把握物质的性质的异同以及组成和用途,注意相关知识的积累,难度不大.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
10.设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A. | 22.4L氯气和氢气的混合气体含有2NA个原子 | |
| B. | 0.1mol/L的NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA | |
| C. | 标准状况下,22.4L乙烯和丙烯的混合气体中含有的碳原子数目为2.5NA | |
| D. | 1molFeI2与1molCl2反应转移的电子数为2NA |
7.含有一个三键的炔烃,加氢后产物的键线式为 ,这种炔烃有( )
,这种炔烃有( )
 ,这种炔烃有( )
,这种炔烃有( )| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
4. 氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生主反应①和副反应②,有关物质产率与温度的关系如图
氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生主反应①和副反应②,有关物质产率与温度的关系如图
4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-905kJ?mol-1 ①
4NH3(g)+3O2(g)?2N2(g)+6H2O(g)△H=-1268kJ?mol-1 ②
下列说法中正确的是( )
 氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生主反应①和副反应②,有关物质产率与温度的关系如图
氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生主反应①和副反应②,有关物质产率与温度的关系如图4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-905kJ?mol-1 ①
4NH3(g)+3O2(g)?2N2(g)+6H2O(g)△H=-1268kJ?mol-1 ②
下列说法中正确的是( )
| A. | 在400℃时,反应①未达平衡,反应②达到平衡 | |
| B. | 800℃后再升高温度,反应①的平衡逆向移动;反应②的平衡正向移动 | |
| C. | 加压可提高NH3生成NO的转化率 | |
| D. | N2氧化为NO的热化学方程式为:N2(g)+O2(g)?2NO(g)△H=-181.5 kJ•mol-1 |
1.根据下图所给信息,得出的结论正确的是( )


| A. | 碳的燃烧热为b kJ/mol | B. | 2C(s)+O2(g)═2CO(g)△H=-2(b-a) kJ/mol | ||
| C. | 2CO2(s)═2CO(g)+O2(g)△H=+a kJ/mol | D. | C(s)+O2(g)═CO2(g)△H<-b kJ/mol |
18. 向甲、乙两个容积均为1L的恒温恒容的密闭容器中,分别充入一定量的SO2和O2发生反应:2SO2(g)+O2(g)?2SO3(g)△H=-197.74kJ•mol-1.其中甲充入2molSO2、1molO2,乙充入1molSO2、0.5molO2,一段时间后达到平衡时,测得两容器中c(SO2)[mol•L-1]随时间t(min)的变化关系如图所示.下列说法正确的是( )
向甲、乙两个容积均为1L的恒温恒容的密闭容器中,分别充入一定量的SO2和O2发生反应:2SO2(g)+O2(g)?2SO3(g)△H=-197.74kJ•mol-1.其中甲充入2molSO2、1molO2,乙充入1molSO2、0.5molO2,一段时间后达到平衡时,测得两容器中c(SO2)[mol•L-1]随时间t(min)的变化关系如图所示.下列说法正确的是( )
 向甲、乙两个容积均为1L的恒温恒容的密闭容器中,分别充入一定量的SO2和O2发生反应:2SO2(g)+O2(g)?2SO3(g)△H=-197.74kJ•mol-1.其中甲充入2molSO2、1molO2,乙充入1molSO2、0.5molO2,一段时间后达到平衡时,测得两容器中c(SO2)[mol•L-1]随时间t(min)的变化关系如图所示.下列说法正确的是( )
向甲、乙两个容积均为1L的恒温恒容的密闭容器中,分别充入一定量的SO2和O2发生反应:2SO2(g)+O2(g)?2SO3(g)△H=-197.74kJ•mol-1.其中甲充入2molSO2、1molO2,乙充入1molSO2、0.5molO2,一段时间后达到平衡时,测得两容器中c(SO2)[mol•L-1]随时间t(min)的变化关系如图所示.下列说法正确的是( )| A. | 压强:p(甲)<2p(乙) | |
| B. | 热量:Q(甲)<2Q(乙) | |
| C. | 乙中前5min内的反应速率v(O2)=0.10mol•L-1•min-1 | |
| D. | 保持其他条件不变,若起始时向乙中充入0.4molSO2、0.2molO2、0.4molSO3,则此时v(正)<v(逆) |
19.下列化学用语书写正确的是( )
| A. | 1个氖原子 Na | B. | +2价的铁元素 Fe+2 | ||
| C. | 2个氢分子 2H | D. | 4个铵根离子 4NH4+ |
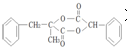 )是一种新型香料的主要成分之一.I的合成路线如下(部分产物和部分反应条件略去):
)是一种新型香料的主要成分之一.I的合成路线如下(部分产物和部分反应条件略去):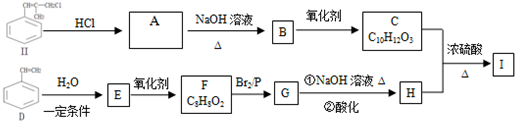

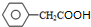 .
. .
. (写结构简式).
(写结构简式).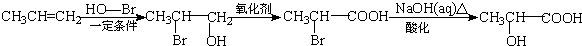 .
.