题目内容
15.化学是实验的学科,按要求回答下列问题.(1)下列四套装置是实验室常见的气体发生装置(不能重复选择):
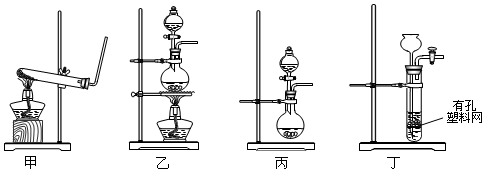
其中可以用于制取氨气的是甲(填编号,下同),反应方程式2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;用于制取NO2的是丙;用于制取Cl2的是乙.
(2)用装置X(下图)可以验证Cl2能使有色布条褪色的真正原因.开始实验时,首先应打开(填“关闭”或“打开”)活塞A.
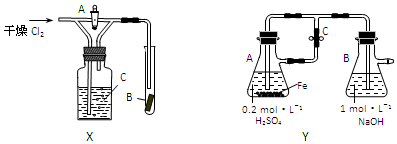
(3)在制取Fe(OH)2时,为了防止Fe(OH)2被O2氧化,通常采用Y装置(上图).开始实验时,首先应打开(填“关闭”或“打开”)止水夹C,A装置中H2SO4和Fe反应生成氢气的作用有两点:一是排走装置中的氧气和NaOH溶液中的溶解氧;二是利用氢气的压强将硫酸亚铁排入B中
(4)用18mol•L-1的浓硫酸,配制100mL 2mol•L-1的硫酸溶液,试回答下列问题.
I.计算需要浓硫酸的体积是11.1mL (保留一位小数)
II.配制时主要有以下五个操作步骤:
①沿烧杯内壁,向盛有30mL蒸馏水的烧杯中慢慢加入浓硫酸,边加边搅拌,并冷却至室温;
②继续往容量瓶中加蒸馏水至液面接近刻度线2cm~3cm:
③将稀释后的溶液沿玻璃棒注入100mL容量瓶中;
④在烧杯中加入少量的蒸馏水,小心洗涤2~3次后移入容量瓶中;
⑤改用胶头滴管加蒸馏水至刻度线.加盖摇匀.
其正确顺序为①③④②⑤ (填序号)
Ⅲ.如果定容时俯视刻度线,则配制溶液的浓度偏低(填“偏低”、“偏高”)
分析 (1)制备氨气为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,制取NO2可选硝酸钠、亚硝酸钠溶液制备,制取Cl2选浓盐酸与二氧化锰反应制备;
(2)验证Cl2能使有色布条褪色的真正原因.利用对比实验说明,开始实验时,首先应打开活塞,后关闭活塞,对比现象;
(3)制取Fe(OH)2时,为了防止Fe(OH)2被O2氧化,通常采用Y装置,先打开C,利用生成的氢气将装置内空气排出,再关闭C,利用氢气的压强将硫酸亚铁排入B中;
(4)I.配制前后溶质的物质的量不变;
II.浓溶液配制溶液时,计算、量取、稀释、冷却、转移、洗涤、定容、摇匀、装瓶;
Ⅲ.如果定容时俯视刻度线,V偏小,结合c=$\frac{n}{V}$分析.
解答 解:(1)制备氨气为固体与固体加热原理,选择甲装置,反应为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,制取NO2可选硝酸钠、亚硝酸钠溶液制备,为液体混合,可选丙装置;制取Cl2选浓盐酸与二氧化锰反应制备,为固体与液体反应加热原理,选择乙装置,
故答案为:甲;2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;丙;乙;
(2)验证Cl2能使有色布条褪色的真正原因.利用对比实验说明,开始实验时,首先应打开活塞,后关闭活塞,对比可知干燥的氯气不能有色布条褪色,
故答案为:打开;
(3)制取Fe(OH)2时,为了防止Fe(OH)2被O2氧化,通常采用Y装置,先打开C,利用生成的氢气将装置内空气排出,再关闭C,利用氢气的压强将硫酸亚铁排入B中,可发生硫酸亚铁与NaOH的反应生成氢氧化亚铁,观察到白色沉淀生成,
故答案为:打开;利用氢气的压强将硫酸亚铁排入B中;
(4)I.用18mol•L-1的浓硫酸,配制100mL 2mol•L-1的硫酸溶液,由配制前后溶质的物质的量不变,可知浓硫酸的体积为$\frac{0.1L×2mol/L}{18mol/L}$=0.0111L=11.1mL,
故答案为:11.1;
II.浓溶液配制溶液时,计算、量取、稀释、冷却、转移、洗涤、定容、摇匀、装瓶,且定容时加水至刻度线2cm~3cm,改用胶头滴管滴加,则正确的步骤为①③④②⑤,
故答案为:①③④②⑤;
Ⅲ.如果定容时俯视刻度线,V偏小,由c=$\frac{n}{V}$可知,配制溶液的浓度偏低,故答案为:偏低.
点评 本题考查物质的制备实验,为高频考点,把握制备原理、实验装置的作用、溶液的配制、实验技能为解答的关键,侧重分析与实验能力的考查,注意元素化合物知识与实验的结合,题目难度不大.

| A. | NaNO2是还原剂 | B. | 生成1个N2时转移的电子数为6个 | ||
| C. | NH4Cl中的N元素被还原 | D. | N2既是氧化产物又是还原产物 |
| A. | Ca2(PO4)3(OH) | B. | Ca5(PO4)3(OH) | C. | Ca4(PO4)3(OH) | D. | Ca3(PO4)3(OH) |
①粗铜与直流电源负极相连
②阴极发生的反应为Cu2++2e-=Cu
③电路中每通过3.0l×1023个电子,得到的精铜质量为16g
④杂质Ag以Ag2SO4的形式沉入电解槽形成“阳极泥”
| A. | ②③ | B. | ②④ | C. | ③④ | D. | ①③ |
| A. | 等浓度的 CH3COOH 与 KOH 任意比混合:c(K+)+c(H+)=c(OH-)+c(CH3COO-) | |
| B. | 在滴有酚酞溶液的氨水里,加入盐酸至恰好呈无色,则此时溶液的 pH=7 | |
| C. | 浓度均为 0.1 mol/L 的氨水和氯化铵溶液,水电离出的 c(H+)前者大于后者 | |
| D. | 常温下 pH 为 5 的盐酸溶液稀释 1000 倍后,pH 等于 8 |
| A. | 如果a1=a2,b1=b2,则混合溶液中c(CH3COO-)=c(Na+) | |
| B. | 如果混合溶液的PH=7,则混合溶液中c(CH3COO-)>c(Na+) | |
| C. | 如果混合溶液的PH<7,则a1b1=a2b2 | |
| D. | 如果a1=a2,且混合溶液的PH<7,则b1>b2 |
| 城市 | 污染指数 | 首要污染物 | 空气质量等级 | ||
| SO2 | NO2 | PM10 | |||
| A | 98 | 23 | 67 | SO2 | Ⅱ |
| B | 47 | 29 | 35 | SO2 | Ⅰ |
| C | 62 | 80 | 113 | PM10 | Ⅲ |
| D | 52 | 76 | 59 | NO2 | Ⅰ |
(2)汽车尾气则是城市大气中氮氧化物的主要来源之一.治理方法之一是在汽车排气管上加装“催化转化器”,使CO与NOx反应生成可参与大气生态环境循环的无毒气体,这些无毒气体是CO2、N2.
(3)SO2的排放是造成酸雨的主要因素.
①若用足量的氢氧化钠溶液吸收含二氧化硫的工业废气,写出该反应的化学反应方程式2NaOH+SO2=Na2SO3+H2O.
②若将含二氧化硫的废气通入水中,在一段时间内连续不断测定溶液的pH值,发现pH值变小,这是由于空气中的氧气也参与了相关反应,表示该变化的化学方程式是2H2SO3+O2=2H2SO4.
| A. | NaBr: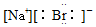 | B. | MgCl2: | C. | KCl: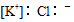 | D. | Na2O2: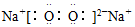 |