题目内容
下列离子方程式正确的是( )
| A、碳酸钙和盐酸反应:CO32-+2H+═H2O+CO2↑ |
| B、向硝酸银溶液中加盐酸:Ag++C1-═AgCl↓ |
| C、向稀盐酸溶液中加铁:3Fe+6H+═3Fe3++3H2↑ |
| D、向氢氧化钡溶液中加硫酸溶液:Ba2++SO42-═BaSO4↓ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.碳酸钙为沉淀,应保留化学式;
B.硝酸银与盐酸反应生成氯化银沉淀和硝酸;
C.不符合反应的客观事实,铁与盐酸反应生成亚铁离子;
D.漏掉氢离子与氢氧根离子的反应.
B.硝酸银与盐酸反应生成氯化银沉淀和硝酸;
C.不符合反应的客观事实,铁与盐酸反应生成亚铁离子;
D.漏掉氢离子与氢氧根离子的反应.
解答:
解:A.碳酸钙和盐酸反应,离子方程式:CaCO3+2H+═H2O+CO2↑+Ca2+,故A错误;
B.向硝酸银溶液中加盐酸,离子方程式:Ag++C1-═AgCl↓,故B正确;
C.向稀盐酸溶液中加铁,反应的离子方程式:Fe+2H+═Fe2++H2↑,故C错误;
D.向氢氧化钡溶液中加硫酸溶液,离子方程式:2OH-+2H++Ba2++SO42-═BaSO4↓+2H2O,故D错误;
故选:B.
B.向硝酸银溶液中加盐酸,离子方程式:Ag++C1-═AgCl↓,故B正确;
C.向稀盐酸溶液中加铁,反应的离子方程式:Fe+2H+═Fe2++H2↑,故C错误;
D.向氢氧化钡溶液中加硫酸溶液,离子方程式:2OH-+2H++Ba2++SO42-═BaSO4↓+2H2O,故D错误;
故选:B.
点评:本题考查了离子方程式的书写,是高考热门考点,明确反应的实质、物质的性质和拆分原则是解题关键,注意反应必须符合客观事实.

练习册系列答案
相关题目
在相同温度时100mL 0.01mol/L的醋酸溶液与10mL 0.1mol/L的醋酸溶液相比较,下列数值前者大于后者的是( )
| A、中和时所需NaOH的量 |
| B、电离程度 |
| C、H+的浓度 |
| D、CH3COOH的物质的量 |
弱电解质电离要吸收热量.分别用40克氢氧化钠和盐酸、醋酸完全反应,放出的热量( )
| A、前者大于后者 | B、相等 |
| C、前者小于后者 | D、无法判断 |
下列原子(离子)的结构示意图错误的是( )
A、磷原子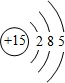 |
B、钠离子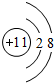 |
C、氧离子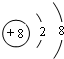 |
D、氢离子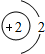 |
下列电离或水解方程式中,正确的是( )
| A、CH3COOH=CH3COO-+H+ |
| B、Br-+H2O?HBr+OH- |
| C、CO32-+2H2O?H2CO3+2OH- |
| D、NH4++H2O?NH3?H2O+H+ |
下列分散系中,属于胶体的是( )
| A、稀硫酸 | B、蛋白质溶液 |
| C、三氯化铁溶液 | D、石灰水 |
 某学生欲用已知物质的量浓度为0.1000mol/L的NaOH溶液来测定未知物质的量浓度的盐酸,选择酚酞作指示剂.请填写下列空白:
某学生欲用已知物质的量浓度为0.1000mol/L的NaOH溶液来测定未知物质的量浓度的盐酸,选择酚酞作指示剂.请填写下列空白: