题目内容
9.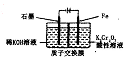 电解法处理酸性含铬废水(主要含有Cr2O72-)时,以铁板作阴、阳极,处理过程中存在反应Cr2O72-+6Fe2+l4H+═2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去,下列说法不正确的是( )
电解法处理酸性含铬废水(主要含有Cr2O72-)时,以铁板作阴、阳极,处理过程中存在反应Cr2O72-+6Fe2+l4H+═2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去,下列说法不正确的是( )| A. | 阳极反应为Fe-2e-=Fe2+ | |
| B. | 在阴极室,发生的电极反应为:Cr2O72-+6e-+7H2O=Cr(OH)3+8OH- | |
| C. | 在阳极室,pH增大会有Fe(OH)3沉淀生成 | |
| D. | 电路中每转移12 mol电子,最多有1 mol Cr2O72- 被还原 |
分析 A.Fe板作阳极,为活性电极,Fe失电子,发生氧化反应生成亚铁离子;
B.阴极发生还原反应,溶液中的氢离子得到电子发生还原反应;
C.在阳极室生成Fe2+,由反应式Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O可知,则在阳极室,消耗氢离子;
D.Fe-2e-=Fe2+,则转移电子数12mol需要6molFe,再根据能够处理的关系式,得6Fe~12e-~6Fe2+~Cr2O72-,据此计算.
解答 解:A.Fe板作阳极,为活性电极,Fe失电子,发生氧化反应生成亚铁离子,阳极反应为Fe-2e-═Fe2+,故A正确;
B.阴极发生还原反应,溶液中的氢离子得到电子发生还原反应,电极反应为:2H++2e-=H2,故B错误;
C.在阳极室生成Fe2+,由反应式Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O可知,则在阳极室,消耗氢离子,溶液的酸性减弱,溶液pH增大,有Fe(OH)3沉淀生成,故C正确;
D.Fe-2e-=Fe2+,则转移电子数12mol需要6molFe,再根据能够处理的关系式,得6Fe~12e-~6Fe2+~Cr2O72-,故被还原的Cr2O72-的物质的量为1mol,故D正确;
故选B.
点评 本题考查电解原理、氧化还原反应等,清楚发生的电极反应是解题的关键,是对学生综合能力的考查,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.下列有关化学用语表示正确的是( )
| A. | NF3的电子式: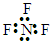 | B. | F-的结构示意图: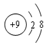 | ||
| C. | 中子数为18的硫原子:${\;}_{16}^{18}$S | D. | 乙酸甲酯的结构简式:HCOOCH2CH3 |
17.短周期元素A、B、C、D的原子序数依次递增,它们的原子序数之和为36,原子最外层电子数之和为14.其中A与C同主族,B与D同主族,A、C原子的最外层电子数之和等于B原子的次外层电子数,下列叙述正确的是( )
| A. | 一定条件下,B单质能置换出D单质,C单质能置换出A单质 | |
| B. | D元素处于元素周期表中第3周期第IVA族 | |
| C. | A、C的最高价氧化物均为离子化合物 | |
| D. | D的氢化物比B的氢化物稳定 |
4.下列实验装置、操作能达到实验目的是( )
| A. | 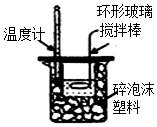 测定中和热 | B. | 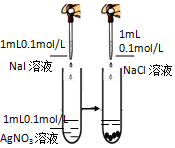 沉淀转化 | ||
| C. | 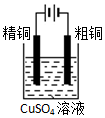 粗铜的电解精炼 | D. | 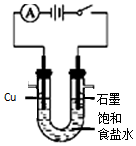 电解食盐水 |
14.已知某水溶液中大量存在H+、Mg2+、K+、NO3-、Cl-中的四种离子,且存在的各离子具有相同的物质的量,则不能存在的离子是( )
| A. | H+ | B. | Mg2+ | C. | Cl- | D. | NO3- |
1.下列离子方程式书写正确的是( )
| A. | H2SO4与 Ba(OH)2 溶液反应:Ba2++SO42-+H++OH-═BaSO4↓+H2O | |
| B. | 金属钠与水的反应:Na+H2O═Na++OH-+H2↑ | |
| C. | 向足量NaHCO3溶液中滴人少量Ca(OH)2溶液:Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32- | |
| D. | 常温下,将氯气通人水中:Cl2+H2O═2H++2Cl-+ClO- |
18.某溶液中含有 HCO3-、CO32-、Na+、NO3-四种离子,若向其中加入 Na2O2 粉末,充分反应后(溶液体积变化忽略不计),溶液中离子浓度保持不变的是( )
| A. | CO32- | B. | CO32-、NO3- | C. | NO3- | D. | CO32-、NO3-、Na+ |