题目内容
17.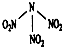 科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如图所示).已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法正确的是( )
科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如图所示).已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法正确的是( )| A. | 分子中N、O间形成的共价键是非极性键 | |
| B. | 分子中四个氮原子共平面 | |
| C. | 该物质既有氧化性又有还原性 | |
| D. | 15.2g该物质含有6.02×1022个原子 |
分析 A.N、O为不同元素;
B.分子中N-N-N键角都是108.1°,则只有3个N原子共面;
C.N(NO2)3中N元素的化合价为+3价;
D.结合n=$\frac{m}{M}$及物质构成计算.
解答 解:A.N(NO2)3是一种共价化合物,N、O原子之间形成的化学键是极性键,故A错误;
B、根据题干信息知该分子中N-N-N键角都是108.1°,推知分子中4个氮原子在空间呈四面体型,所以分子中四个氧原子不可能共平面,故B错误;
C、该分子中的氮元素为+3价,为中间价可失去或得到电子,则该物质既有氧化性又有还原性,故C正确;
D、N(NO2)3的相对分子质量为152,15.2 g N(NO2)3为0.1mol,该物质的分子中所含原子为1NA即6.02×1023个原子,故D错误;
故选C.
点评 本题考查化学键及氧化还原反应,为高频考点,为2011年的安徽理综高考题,把握化学键的判断、氧化还原反应、物质的量的计算为解答的关键,侧重分析与应用能力的考查,综合性较强,题目难度不大.

练习册系列答案
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目
8.下列说法正确的是( )
| A. | 用酸性高锰酸钾溶液可以鉴别己烯、甲苯和苯 | |
| B. | 用系统命名法命名的顺-2-丁烯、反-2-丁烯分别与HCl加成,产物的结构不同 | |
| C. | 聚乳酸(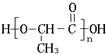 )分子中存在酯基、羧基、羟基 )分子中存在酯基、羧基、羟基 | |
| D. | 有机物CH3CO18OH和C2H5OH在浓硫酸催化作用下产物为CH3CO18OC2H5和H2O |
5.下列溶液中各微粒的浓度关系不正确的是( )
| A. | 0.1 mol/LCH3COOH溶液中:c(CH3COO-)+c(CH3COOH)=0.1mol/L | |
| B. | 将0.2 mol/L NaA溶液和0.1 mol/L盐酸等体积混合所得碱性溶液中:c(Na+)+c(H+)=c(A-)+c(Cl-) | |
| C. | CH3COONa溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| D. | Na2S溶液中:c(Na+)=2(c(S2-)+c(HS-)+c(H2S)) |
12.下列叙述中正确的是( )
| A. | pH=11的Na0H和Na2S溶液中水的电离程度前者大于后者 | |
| B. | 实验室配制氯化亚铁溶液时,将氯化亚铁先溶解在盐酸中,然后用蒸馏水稀释并加入少量铁粉 | |
| C. | 25℃,Cu(OH)2在水中的溶度积和溶解度比其在Cu(NO3)2溶液中的大 | |
| D. | 向FeCl3+3KSCN?Fe(SCN)3+3KCl平衡体系中加入少量KCl 固体,溶液血红色变浅 |
2.日常生活中使用的购物袋的材料多为聚乙烯,下列说法中正确的是( )
| A. | 用纯净的乙烯合成的聚乙烯是纯净物 | |
| B. | 聚乙烯可以人工合成,也可以是天然高分子化合物 | |
| C. | 聚乙烯能使酸性高锰酸钾溶液褪色 | |
| D. | 聚乙烯的单体能够使溴的四氯化碳溶液褪色 |
9.油脂皂化后,使肥皂和甘油充分分离,可以采用( )
| A. | 萃取 | B. | 蒸馏 | C. | 过滤 | D. | 盐析 |
6.某元素的一种同位素X原子的质量数为A,含N个中子,它与1H原子组成HmX分子,在ag HmX分子中含电子的物质的量是( )
| A. | $\frac{a}{A+m}$(A-N+m)mol | B. | $\frac{a}{A}$(A-N)mol | C. | $\frac{a}{A+m}$(A-N)mol | D. | $\frac{a}{A}$(A-N+m)mol |
17.以下关于生活中常见的几种有机物的说法正确的是( )
| A. | PVC(聚氯乙烯)是生活中常用的一种管材,其中聚氯乙烯中含有碳碳双键结构,所以可以使溴水褪色 | |
| B. | 乙炔可以作为氧炔焰的原料气体,是因为其燃烧时火焰的温度很高 | |
| C. | 聚乙烯常用于制造生活常见的塑料制品,其中聚乙烯属于纯净物 | |
| D. | 氯仿(三氯甲烷)是工业上常用的一种溶剂,一般用甲烷和氯气按1:3反应即可生成纯净的氯仿 |