题目内容
某二价金属氢氧化物溶液加入过量NaHCO3溶液,生成二价金属碳酸盐沉淀,经过滤所得沉淀烘干后称得其质量为39.4g;将沉淀与足量盐酸反应,生成气体4.48L.取滤液的
恰好与1mol/L的盐酸70mL完全反应,收集到气体1.12L(标准状况).回答:
(1)39.4g沉淀的物质的量 ;
(2)二价金属的相对原子质量 ;
(3)加入NaHCO3的质量 .
| 1 |
| 10 |
(1)39.4g沉淀的物质的量
(2)二价金属的相对原子质量
(3)加入NaHCO3的质量
考点:化学方程式的有关计算
专题:计算题
分析:根据MCO3沉淀39.4g经过滤、洗涤干燥后与足量的稀盐酸充分反应后收集到在标准状况下的4.48L气体为二氧化碳,利用该反应的化学方程式可知,可计算金属M的相对原子质量以及沉淀的物质的量,根据滤液碳酸钠和盐酸之间的反应计算加入NaHCO3的质量.
解答:
解:(1)某二价金属氢氧化物溶液加入过量NaHCO3溶液,发生反应:M2++2OH-+2HCO3-=MCO3+CO32-+2H2O,生成二价金属碳酸盐沉淀MCO3,其质量为39.4g;洗涤干燥后与足量的稀盐酸充分反应后收集到在标准状况下的4.48L即0.2mol二氧化碳,根据碳元素守恒,所以沉淀MCO3的物质的量是0.2mol,故答案为:0.2mol;
(2)质量为39.4g沉淀的物质的量是0.2mol,其摩尔质量是197g/mol,所以二价金属的相对原子质量为197-12-48=137,故答案为:137;
(3)根据反应:M2++2OH-+2HCO3-=MCO3+CO32-+2H2O,滤液是生成的0.2mol碳酸钠和剩余碳酸氢钠的混合物,取滤液的
与1mol/L的盐酸70mL即0.07mol盐酸完全反应,收集到气体1.12L(标准状况)即0.05mol的二氧化碳,所以碳酸氢钠的物质的量是0.03mol,原碳酸氢钠的剩余量是0.3mol,消耗碳酸氢钠是0.1mol,共加入加入NaHCO3的物质的量是0.4mol,质量是33.6g,故答案为:33.6g.
(2)质量为39.4g沉淀的物质的量是0.2mol,其摩尔质量是197g/mol,所以二价金属的相对原子质量为197-12-48=137,故答案为:137;
(3)根据反应:M2++2OH-+2HCO3-=MCO3+CO32-+2H2O,滤液是生成的0.2mol碳酸钠和剩余碳酸氢钠的混合物,取滤液的
| 1 |
| 10 |
点评:本题考查学生元素以及化合物的性质知识,注意反应的实质以及方程式的应用,难度较大.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
已知:Fe2+结合S2-的能力大于结合OH-的能力,而Al3+则正好相反,I2的氧化性比S强.在Fe2(SO4)3和AlCl3的混合溶液中,先加入过量的KI溶液,再加入足量的Na2S溶液,所得沉淀是( )
| A、Fe2S3和 Al(OH)3 |
| B、Fe(OH)3和Al(OH)3 |
| C、FeS、Al(OH)3 和S |
| D、Al2S3、FeS和S |
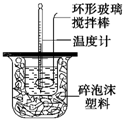 在量热器中将50ml、0.50mol?L-1CH3COOH溶液与50ml、0.55mol?L-1NaOH溶液混合,温度从25.16℃升高到27.46℃.已知量热计的热容常数(量热计各部件每升高10C所需的热量)是150J?0C-1,C=4.18J?g-1?0C-1,溶液的密度为1g?cm-3.
在量热器中将50ml、0.50mol?L-1CH3COOH溶液与50ml、0.55mol?L-1NaOH溶液混合,温度从25.16℃升高到27.46℃.已知量热计的热容常数(量热计各部件每升高10C所需的热量)是150J?0C-1,C=4.18J?g-1?0C-1,溶液的密度为1g?cm-3. 液,试画出原电池的装置图,并说明其工作原理.
液,试画出原电池的装置图,并说明其工作原理.