题目内容
13.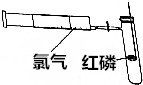 已知SnCl4、SiCl4、AlCl3、PCl3、PCl5等氯化物在潮湿的空气中都有白雾生成.为清楚地观察磷在氯气中燃烧,达到PCl3和PCl5分步生成的目的,可预先把干燥的氯气贮存在100mL的注射器内,再把火柴头大小的红磷置于玻璃燃烧匙上烘干后组成如图所示的装置.
已知SnCl4、SiCl4、AlCl3、PCl3、PCl5等氯化物在潮湿的空气中都有白雾生成.为清楚地观察磷在氯气中燃烧,达到PCl3和PCl5分步生成的目的,可预先把干燥的氯气贮存在100mL的注射器内,再把火柴头大小的红磷置于玻璃燃烧匙上烘干后组成如图所示的装置.操作时打开弹簧夹,缓缓推动注射器的活塞,待磷燃烧出现白雾时,立即关闭弹簧夹,停止推入氯气,片刻后,可见到试管内白雾凝成无色液滴附着在试管内壁.然后再打开弹簧夹,继续推入Cl2就可看到管壁上液滴逐渐消失,管内出现白烟.最后白烟凝结成白色固体附着在试管内壁上.试回答:
(1)该实验选择玻璃燃烧匙,不选其他金属燃烧匙的原因是氯气的氧化性很强,能与金属反应生成氯化物,影响实验效果.
(2)该实验的关键是使用的氯气和红磷必须干燥.请用必要的文字和化学方程式说明其原因氯气与磷反应生成的三氯化磷和五氯化磷易与水反应,PCl3+3H2O=H3PO3+3HCl,PCl5+4H2O=H3PO4+5HCl,致使实验始终看不到白色固体附着.
(3)因第二次推入氯气时发生的反应是PCl3+Cl2=PCl5(用化学方程式表示),故第一次推入氯气要缓缓进行的原因是避免氯气推入量过多,生成五氯化磷,看不到白雾冷却后,凝结为无色液体现象.
分析 (1)氯气的氧化性很强,能与金属反应生成氯化物;
(2)氯化物在潮湿的空气中都有白雾生成,说明氯化物与水发生反应生成氯化氢气体,干拢实验现象;
(3)白磷与少量氯气反应生成PCl3,PCl3为气体,所以试管内的白雾冷凝成无色液滴附着在试管内壁,PCl3再与氯气反应生成PCl5,PCl5为白色固体,所以管内出现白烟,最后白烟凝结成白色固体附着在试管内壁上.
解答 解:(1)氯气的氧化性很强,能与金属反应生成氯化物,所以实验选择玻璃燃烧匙,不选其他金属燃烧匙,
故答案为:氯气的氧化性很强,能与金属反应生成氯化物,影响实验效果;
(2)氯化物在潮湿的空气中都有白雾生成,说明氯化物与水发生反应生成氯化氢气体,干拢实验现象,如PCl3+3H2O=H3PO3+3HCl,PCl5+4H2O=H3PO4+5HCl,
故答案为:氯气与磷反应生成的三氯化磷和五氯化磷易与水反应,PCl3+3H2O=H3PO3+3HCl,PCl5+4H2O=H3PO4+5HCl,致使实验始终看不到白色固体附着;
(3)白磷与少量氯气反应生成PCl3,PCl3为气体,所以试管内的白雾冷凝成无色液滴附着在试管内壁,PCl3再与氯气反应生成PCl5,PCl3+Cl2=PCl5,PCl5为白色固体,所以管内出现白烟,最后白烟凝结成白色固体附着在试管内壁上,故第一次推入氯气要缓缓进行的原因是避免氯气推入量过多,生成五氯化磷,看不到白雾冷却后,凝结为无色液体现象,
故答案为:PCl3+Cl2=PCl5;避免氯气推入量过多,生成五氯化磷,看不到白雾冷却后,凝结为无色液体现象.
点评 本题考查白磷与氯气的反应,难点是反应物的量不同产物不同,增强对题中信息进行分析加工的能力是解此类题的关键,难度适中.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
3.下列各组物质中不属于同素异形体的是( )
| A. | 金刚石、石墨 | B. | 红磷、白磷 | ||
| C. | 一氧化氮与二氧化氮 | D. | 氧气、臭氧 |
8. 一定温度下,密闭容器内某一反应中X、Y的物质的量随反应时间变化的曲线如图所示,下列叙述中不正确的是( )
一定温度下,密闭容器内某一反应中X、Y的物质的量随反应时间变化的曲线如图所示,下列叙述中不正确的是( )
 一定温度下,密闭容器内某一反应中X、Y的物质的量随反应时间变化的曲线如图所示,下列叙述中不正确的是( )
一定温度下,密闭容器内某一反应中X、Y的物质的量随反应时间变化的曲线如图所示,下列叙述中不正确的是( )| A. | 反应的化学方程式为:2X?Y | B. | t1时,Y的浓度是X浓度的2倍 | ||
| C. | t2时,正反应速率大于逆反应速率 | D. | t3时,正逆反应速率相等,达到平衡 |
18.下列叙述正确的是( )
| A. | Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应 | |
| B. | 足量的Fe在Cl2中燃烧生成FeCl2和FeCl3 | |
| C. | 先后将等物质的量的Fe2O3和Fe分别溶于同一稀盐酸时无气体放出 | |
| D. | Fe2O3$\stackrel{HCl(aq)}{→}$FeCl3(aq)$\stackrel{△}{→}$无水FeCl3,在给定的条件下能实现转化 |
5.在铜的催化作用下氨气和氟气反应,得到两种氟化物,一种是离子化合物M,另一种是共价化合物N且其分子构型与氨气类似,下列有关说法错误的是( )
| A. | 该反应中氧化剂与还原剂物质的量之比为3:4 | |
| B. | 该反应中氧化产物与还原产物物质的量之比为1:4 | |
| C. | N是氧化产物,而且是极性分子 | |
| D. | M是还原产物,其还原性比NH3弱 |
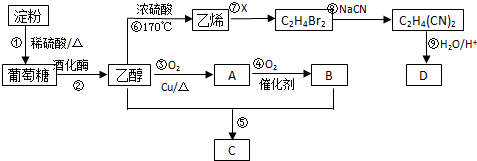
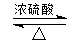 CH3COOCH2CH3+H2O.反应⑥用于实验室制乙烯,为除去其中可能混有的SO2应选用的试剂是NaOH溶液.
CH3COOCH2CH3+H2O.反应⑥用于实验室制乙烯,为除去其中可能混有的SO2应选用的试剂是NaOH溶液.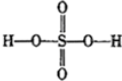 过硫酸:
过硫酸: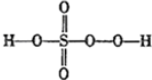
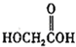 (b)
(b)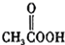 (c)H2O2(d)
(c)H2O2(d) (e)
(e) (f)
(f)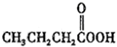 (g)O3(h)
(g)O3(h)