题目内容
下列有关电解质溶液中粒子浓度关系正确的是
A.pH=1的NaHSO4溶液:c(H+)=c(SO42-)十c(OH-)
B.25℃时,pH为9的Na2CO3溶液和pH为5的NaHSO4溶液中,水的电离程度相同
C.CO2的水溶液:c(H+)>c(HCO3-)=2c(CO32-)
D.含等物质的量的NaHC2O4和Na2C2O4的溶液:3c(Na+)=2[c(HC2O4-)+ c(C2O42-)+c(H2C2O4)]
A
【解析】
试题分析:根据物料守恒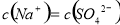 ,根据电荷守恒
,根据电荷守恒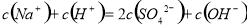 ,所以c(H+)=c(SO42-)十c(OH-),故A正确;pH为9的Na2CO3溶液,水的电离的氢离子为10-5mol/L;pH为5的NaHSO4溶液,水的电离的氢离子为10-9mol/L,故B错误;碳酸的第二步电离不第一步电离弱的多,c(HCO3-)远大于c(CO32-),故C错误;根据物料守恒,2c(Na+)=3[c(HC2O4-)+ c(C2O42-)+c(H2C2O4)],故D错误。
,所以c(H+)=c(SO42-)十c(OH-),故A正确;pH为9的Na2CO3溶液,水的电离的氢离子为10-5mol/L;pH为5的NaHSO4溶液,水的电离的氢离子为10-9mol/L,故B错误;碳酸的第二步电离不第一步电离弱的多,c(HCO3-)远大于c(CO32-),故C错误;根据物料守恒,2c(Na+)=3[c(HC2O4-)+ c(C2O42-)+c(H2C2O4)],故D错误。
考点:本题考查弱电解质电离和盐的水解。

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目
 H++OH-,向右移动且溶液呈酸性的是
H++OH-,向右移动且溶液呈酸性的是