题目内容
6.下列实验装置进行相应的实验,不能达到实验目的是( )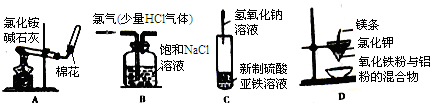
| A. | 实验室制取并收集氨气 | B. | 除去Cl2中的HCl气体杂质 | ||
| C. | 实验室制取氢氧化亚铁 | D. | 铝热反应实验 |
分析 A.氯化铵和氢氧化钙在加热条件下反应生成氨气;
B.氯气中的杂质氯化氢能溶于饱和食盐水中,而氯气不能溶于食盐水中;
C.氢氧化亚铁易被空气中的氧气氧化;
D.镁与氧气反应生成氧化镁,放热大量热,铝热反应中镁带起到了引燃剂的作用;氯酸钾受热分解生成氧气起助燃的作用.
解答 解:A.氯化铵和氢氧化钙在加热条件下反应生成氨气,氨气的密度比空气小,可用向下排空法收集,故A正确;
B.氯气中的杂质氯化氢能溶于饱和食盐水中,而氯气不能溶于食盐水中,将混合气体通入饱和食盐水中,可以采用洗气的方法来分离,故B正确;
C.氢氧化亚铁易被空气中的氧气氧化,应隔绝空气制备,故C错误;
D.镁与氧气反应生成氧化镁,放热大量热,铝热反应中镁带起到了引燃剂的作用;氯酸钾受热分解生成氧气起助燃的作用,不能用氯化钾,故D错误.
故选CD.
点评 本题考查化学实验方案的评价,涉及物质制备、除杂以及铝热反应,题目难度中等,注意掌握铝热反应原理,明确合金特点及金属铁、镁的化学性质,试题侧重考查学生的分析、理解能力及化学实验能力.

练习册系列答案
相关题目
17.对于金属冶炼的工业方法,下列有关说法中正确的是( )
| A. | 可用电解饱和的MgCl2溶液的方法获得金属镁 | |
| B. | 电解CuSO4溶液精炼金属铜时,用铁做阳极 | |
| C. | 电解熔融Al2O3方法冶炼金属铝时,同时要加入冰晶石作助熔剂 | |
| D. | 工业上常采用活泼金属还原法冶炼金属银 |
14.对下图有机物的命名正确的是( )
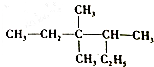

| A. | 2-乙基-3,3-二,甲基戊烷 | |
| B. | 3,3,4-三甲基己烷 | |
| C. | C的价电子轨道表示式:3,3-甲基-4乙基戊烷 | |
| D. | 2,3,3-三甲基己烷 |
11.下列叙述正确的是( )
| A. | CaCO3不溶于水,所以CaCO3不是电解质 | |
| B. | 分解反应不一定是氧化还原反应 | |
| C. | 盐、碱一定含有金属元素 | |
| D. | 在水溶液中电离产生H+的化合物一定是酸 |
18.某课外兴趣小组刚收集到一瓶当地的酸雨,计划通过实验检测酸雨的主要成分进而分析探讨当地酸雨的成因.
I.同学们首先对当地酸雨的成因提出假设
假设1.空气中含有的过多的氮氧化物造成的;
假设2.空气中含有的过多的二氧化硫造成的;
假设3.空气中过多的氮氧化物、二氧化硫共同造成的.
一组同学设计实验验证假设1,请在下表空白处填写相关实验现象.
其中涉及的化学反应的离子方程式是Cu+4H++2NO3-$\frac{\underline{\;\;△\;\;}}{\;}$Cu2++2NO2↑+2H2O(或3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O).
另一组同学验证假设2,取适量样品并向其中加入盐酸酸化的BaCl2溶液,没有看到白色沉淀生成,该小组得出结论:假设2不成立,你认为是否合理?不合理(填“合理”或“不合理”,如果填“合理”,本小题余下的空不需要填写).如果不合理,请说明原因因为BaCl2与溶液中可能存在的SO32-反应生成的沉淀可溶解于盐酸中.你认为合理的实验验证方案取适量样品,加入适量Ba(OH)2溶液.
I.同学们首先对当地酸雨的成因提出假设
假设1.空气中含有的过多的氮氧化物造成的;
假设2.空气中含有的过多的二氧化硫造成的;
假设3.空气中过多的氮氧化物、二氧化硫共同造成的.
一组同学设计实验验证假设1,请在下表空白处填写相关实验现象.
| 实验步骤 | 实验现象 | 结论 |
| 取适量样品加热浓缩后加入试管中,再加入适量硫酸和铜片,加热. | 假设1成立 |
另一组同学验证假设2,取适量样品并向其中加入盐酸酸化的BaCl2溶液,没有看到白色沉淀生成,该小组得出结论:假设2不成立,你认为是否合理?不合理(填“合理”或“不合理”,如果填“合理”,本小题余下的空不需要填写).如果不合理,请说明原因因为BaCl2与溶液中可能存在的SO32-反应生成的沉淀可溶解于盐酸中.你认为合理的实验验证方案取适量样品,加入适量Ba(OH)2溶液.
16.下列对应关系不正确的是( )
| 选项 | A | B | C | D |
| 中心原子所在族 | ⅣA族 | ⅤA族 | ⅣA族 | ⅥA族 |
| 分子通式 | AB4 | AB3 | AB2 | AB2 |
| 立体构型 | 正四面体形 | 平面三角形 | 直线形 | V形 |
| A. | A | B. | B | C. | C | D. | D |
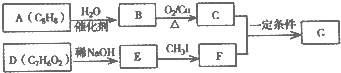
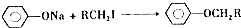

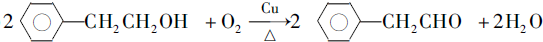 .
. .
.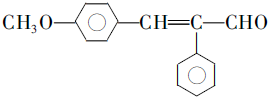 .
.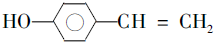 (写结构简式).
(写结构简式).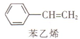
 .
.
 .
.