题目内容
3.下列是中学常见的一些物质之间的转化关系(其中部分反应产物省略),其中I是一种金属单质,A是一种黄绿色的非金属单质;F、M、N均为难溶于水的白色沉淀物质,M和N不溶于稀硝酸;B是一种具有刺激性气味的气体,且具有漂白性;C和D是中学化学中两种常见的强酸.请回答下列问题: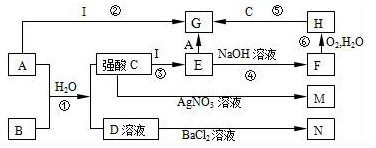
(1)写出物质N的化学式:BaSO4;
(2)写出E→G转化反应的离子方程式:2Fe2++Cl2=2Fe3++2Cl-;
(3)写出反应⑥的化学方程式:4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(4)写出反应①的离子方程式:SO2+Cl2+2H2O=4H++SO42-+2Cl-.
分析 A是一种黄绿色的非金属单质,应为Cl2,M和N不溶于稀硝酸,可知M为AgCl,N为BaSO4,则B应为SO2,是一种具有刺激性气味的气体,且具有漂白性,则C为HCl,D为H2SO4,由转化关系可知I为Fe,E为FeCl2,F为4Fe(OH)2,H为Fe(OH)3,G为FeCl3,结合对应物质的性质以及题目要求可解答该题.
解答 解:A是一种黄绿色的非金属单质,应为Cl2,M和N不溶于稀硝酸,可知M为AgCl,N为BaSO4,则B应为SO2,是一种具有刺激性气味的气体,且具有漂白性,则C为HCl,D为H2SO4,由转化关系可知I为Fe,E为FeCl2,F为4Fe(OH)2,H为Fe(OH)3,G为FeCl3,
(1)由以上分析可知N为BaSO4,故答案为:BaSO4;
(2)FeCl2具有还原性,可与Cl2反应,反应的离子方程式为2Fe2++Cl2=2Fe3++2Cl-,故答案为:2Fe2++Cl2=2Fe3++2Cl-;
(3)Fe(OH)2不稳定,可与氧气发生氧化还原反应,反应的化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(4)反应①是氯气和二氧化碳在水溶液中发生氧化还原反应生成硫酸和盐酸,反应的离子方程式为:SO2+Cl2+2H2O=4H++SO42-+2Cl-,
故答案为:SO2+Cl2+2H2O=4H++SO42-+2Cl-.
点评 本题考查无机物的推断,为高频考点,把握物质的性质、发生的反应为解答的关键,侧重分析与推断能力的考查,注意元素化合物知识的应用,题目难度中等.

练习册系列答案
相关题目
14.一种微生物燃料电池的结构示意图如图所示,关于该电池的叙述不正确的是( )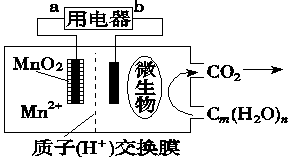

| A. | 电池工作时,电子由b流向a | |
| B. | 正极反应式为:MnO2+4H++2e-═Mn2++2H2O | |
| C. | 放电过程中,H+从负极区移向正极区 | |
| D. | 微生物所在电极区放电时发生还原反应 |
11.室温下,某溶液中由水电离出的H+和OH-物质的量浓度乘积为1×10-24,该溶液中一定不能大量共存的是
( )
( )
| A. | AlO2- | B. | Fe3+ | C. | HCO3- | D. | NH4+ |
18.用NA表示阿伏加德罗常数的值.下列说法不正确的是( )
| A. | H2O2分解产生1molO2,转移的电子数为4NA | |
| B. | 1.00mol NaCl中,所有Na+的最外层电子总数约为8 NA | |
| C. | 常温常压下,4.4gCO2与N2O混合气体中含有的原子总数为0.3NA | |
| D. | 标准状况下,2.24LCH4所含电子数为NA |
15.不能使橙色溴水层变为无色的是( )
| A. | NaOH溶液 | B. | 用CCl4多次萃取 | C. | 锌粉 | D. | KI 溶液 |
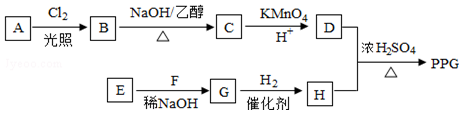
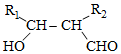
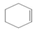 在酸性高锰酸钾溶液中反应生成HOOCCH2CH2CH2CH2COOH
在酸性高锰酸钾溶液中反应生成HOOCCH2CH2CH2CH2COOH .
. .
.
 :
: