题目内容
下列反应所得溶液中一定只含一种溶质的是( )
| A、向稀硝酸中加入铁粉 |
| B、向氯化铝溶液中加入过量的氨水 |
| C、向NaOH溶液中通入CO2气体 |
| D、向MgSO4、H2SO4的混合液中加入过量的Ba(OH)2溶液 |
考点:硝酸的化学性质,镁、铝的重要化合物,铁的化学性质
专题:元素及其化合物
分析:A、向稀硝酸中加入铁粉可生成Fe(NO3)2、Fe(NO3)3等;
B、氢氧化铝不溶于氨水;
C、向NaOH溶液中通入CO2气体,可生成Na2CO3或NaHCO3等物质;
D、向MgSO4、H2SO4的混合液中加入过量的Ba(OH)2溶液,反应生成Mg(OH)2和BaSO4沉淀;
B、氢氧化铝不溶于氨水;
C、向NaOH溶液中通入CO2气体,可生成Na2CO3或NaHCO3等物质;
D、向MgSO4、H2SO4的混合液中加入过量的Ba(OH)2溶液,反应生成Mg(OH)2和BaSO4沉淀;
解答:
解:A、向稀硝酸中加入铁粉,如Fe过量,溶液中可能存在Fe(NO3)2、Fe(NO3)3等溶质,如Fe不足,则存在HNO3、Fe(NO3)3,故A错误;
B、氨水是弱碱,不能溶解氢氧化铝,氯化铝溶液加入过量氨水的反应方程式为:AlCl3+3NH3?H2O═Al(OH)3↓+3NH4Cl,反应所得的溶液中溶质为过量的一水合氨和产物NH4Cl,故B错误;
C、向NaOH溶液中通入CO2气体,当CO2过量时,可能生成Na2CO3或NaHCO3等物质,故C错误;
D、向MgSO4、H2SO4的混合液中加入过量的Ba(OH)2溶液,反应生成Mg(OH)2和BaSO4沉淀,最后溶液中只有过量的Ba(OH)2,只有一种溶质,故D正确;
故选:D.
B、氨水是弱碱,不能溶解氢氧化铝,氯化铝溶液加入过量氨水的反应方程式为:AlCl3+3NH3?H2O═Al(OH)3↓+3NH4Cl,反应所得的溶液中溶质为过量的一水合氨和产物NH4Cl,故B错误;
C、向NaOH溶液中通入CO2气体,当CO2过量时,可能生成Na2CO3或NaHCO3等物质,故C错误;
D、向MgSO4、H2SO4的混合液中加入过量的Ba(OH)2溶液,反应生成Mg(OH)2和BaSO4沉淀,最后溶液中只有过量的Ba(OH)2,只有一种溶质,故D正确;
故选:D.
点评:本题考查元素化合物知识,题目难度不大,本题注意把握常见元素化合物的性质.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
反应过程中固体物质质量增加的是 ( )
| A、氨气通过无水氯化钙粉末 |
| B、氢气通过灼热的氧化铜粉末 |
| C、铝与氧化铁发生铝热反应 |
| D、将锌粒投入到硝酸铜溶液中 |
下列反应中必须加入氧化剂才能进行的是( )
| A、Cl2→Cl- |
| B、Zn→Zn2+ |
| C、KClO3→KCl |
| D、CuO→CuCl2 |
下列哪一个反应表示二氧化硫被还原( )
| A、SO2+2H2O+Cl2=H2SO4+2HCl |
| B、SO2+2NaOH=Na2SO3+H2O |
| C、SO2+2H2S=2H2O+3S↓ |
| D、SO2+PbO2=PbSO4 |
下列说法不正确的是( )
| A、SO2、Na2O2、活性炭都能使品红溶液褪色,但原理不同 |
| B、水在3.98℃时,主要以(H2O)2存在,这两个水分子间是以共价键相结合 |
| C、放热反应 的反应速率,不一定比吸热反应的反应速快 |
| D、同温同压下,3mol C2H4(g)和1mol CO(g)的密度相等 |

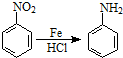 .2CH3CHO
.2CH3CHO