题目内容
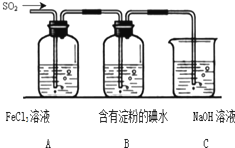 为探究SO2气体的还原性某兴趣小组设计了如图装置图:
为探究SO2气体的还原性某兴趣小组设计了如图装置图:(1)证明SO2与Fe3+发生反应的现象为
(2)实验中所需的SO2气体可以用浓硫酸和铜反应来制取,该反应的化学方程式为
(3)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入KMnO4溶液,不变红,紫色褪去.
方案②:往第二份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红
方案③:往第三份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀
上述方案中不合理的是
考点:性质实验方案的设计,二氧化硫的化学性质
专题:
分析:(1)根据SO2与Fe3+发生反应的反应物、生成物的性质分析解答;
(2)铜与浓硫酸在加热条件下反应生成硫酸铜、二氧化硫和水;
(3)二氧化硫、Fe2+具有还原性,和氧化剂能发生氧化还原反应,能使高锰酸钾溶液现象明显.
(2)铜与浓硫酸在加热条件下反应生成硫酸铜、二氧化硫和水;
(3)二氧化硫、Fe2+具有还原性,和氧化剂能发生氧化还原反应,能使高锰酸钾溶液现象明显.
解答:
解:(1)SO2与Fe3+发生反应SO2+2Fe3++2H2O=SO42-+2Fe2++4H+,原来为黄色铁离子溶液,被二氧化硫还原成浅绿色的亚铁离子溶液,
故答案为:A中溶液由黄色变为浅绿色;
(2)铜与浓硫酸在加热条件下反应生成硫酸铜、二氧化硫和水,反应的方程式为:Cu+2H2SO4(浓)
CuSO4+2H2O+SO2↑,
故答案为:Cu+2H2SO4(浓)
CuSO4+2H2O+SO2↑;
(3)二氧化硫有还原性,高锰酸钾有强氧化性,二氧化硫能与高锰酸钾发生氧化还原反应使高锰酸钾溶液褪色,Fe2+也使高锰酸钾溶液褪色,所以上述方案中不合理的是①,故答案为:方案①;因为A的溶液中含有SO2,SO2也能使KMnO4溶液褪色.
故答案为:A中溶液由黄色变为浅绿色;
(2)铜与浓硫酸在加热条件下反应生成硫酸铜、二氧化硫和水,反应的方程式为:Cu+2H2SO4(浓)
| ||
故答案为:Cu+2H2SO4(浓)
| ||
(3)二氧化硫有还原性,高锰酸钾有强氧化性,二氧化硫能与高锰酸钾发生氧化还原反应使高锰酸钾溶液褪色,Fe2+也使高锰酸钾溶液褪色,所以上述方案中不合理的是①,故答案为:方案①;因为A的溶液中含有SO2,SO2也能使KMnO4溶液褪色.
点评:本题考查的是二氧化硫的性质及实验室制法,注意二氧化硫有还原性,与强氧化剂发生氧化还原反应,还具有漂白性,题目难度不大.

练习册系列答案
相关题目
化学与人类生活密切相关.下列说法中不正确的是( )
| A、伦敦奥运会中采用的新型氢动力计程车可以降低PM2.5的排放,减小大气污染 |
| B、酸雨就是pH<7的雨水,主要是由大气中的SO2、NO2等造成的 |
| C、绚丽缤纷的烟花中添加了含钾、钠、钙、铜等金属元素的化合物 |
| D、服用铬含量超标的药用胶囊会对人体健康造成危害 |
下列关于碳酸钠和碳酸氢钠的比较中,正确的是( )
| A、二者在水中的溶解度不同,碳酸氢钠的溶解度大于碳酸钠的溶解度 |
| B、二者热稳定性不同,碳酸氢钠的热稳定性大于碳酸钠的热稳定性 |
| C、二者都能与盐酸反应放出二氧化碳气体,但碳酸钠生成的气体的速率更快 |
| D、等浓度时,碳酸钠溶液的PH大于碳酸氢钠溶液的PH |
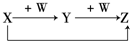 X、Y、Z、W有如图所示的转化关系,则X、W可能是( )
X、Y、Z、W有如图所示的转化关系,则X、W可能是( )①C、O2 ②AlCl3、NaOH ③Fe、HNO3 ④CO2、NaOH.
| A、①②③ | B、①② |
| C、③④ | D、①②③④ |
碱性电池具有容量大、放电电流大的特点,因而得到广泛使用,锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应为:Zn(s)+2MnO2(s)+H2O(l)﹦Zn(OH)2(s)+Mn2O3(s)下列说法错误的是( )
| A、电池工作时,锌失去电子 |
| B、反应时化学能转化为电能 |
| C、电池工作时,电子由正极通过外电路流向负极 |
| D、外电路中每通过0.2mol电子,锌的质量理论上减小6.5g |
维胺酯(Viaminati),治疗各种痤疮、角化异常性皮肤病,结构如图.下列有关维胺酯说法不正确的是( )
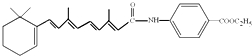

| A、不溶于水,服用后在胃酸作用下能水解 |
| B、在氢氧化钠溶液中水解,1mol维胺酯最多消耗氢氧化钠2mol |
| C、能发生加聚、加成、酯化等反应 |
| D、一定条件下,与溴的四氯化碳反应,1mol维胺酯最多消耗溴5mol |