题目内容
20.已知HCl和NH3均极易溶于水,同温通同压下,用体积为1L的圆底烧瓶分别收集HCl和NH3,将两烧瓶倒立在水槽中,a烧瓶内迅速充满水,b烧瓶内水充满3/4,溶质均未向水槽内扩散,所得盐酸和氨水的浓度分别记为a和b,则a、b关系为( )| A. | a>b | B. | a=b | C. | a<b | D. | 不能确定 |
分析 用体积为1L的圆底烧瓶分别收集HCl和NH3,将两烧瓶倒立在水槽中,a烧瓶内迅速充满水,b烧瓶内水充满$\frac{3}{4}$,则a烧瓶收集满HCl,b烧瓶收集$\frac{3}{4}$NH3,相同条件下,二者物质的量之比为4:3,结合c=$\frac{n}{V}$分析判断.
解答 解:用体积为1L的圆底烧瓶分别收集HCl和NH3,将两烧瓶倒立在水槽中,a烧瓶内迅速充满水,b烧瓶内水充满$\frac{3}{4}$,则a烧瓶收集满HCl,b烧瓶收集$\frac{3}{4}$NH3,相同条件下,二者物质的量之比为4:3,又体积之比为4:3,所以结合c=$\frac{n}{V}$可知,所得溶液的浓度相等,即a=b,故选B.
点评 本题考查物质的量浓度计算,比较基础,判断氨气与HCl的物质的量之比是关键,注意对公式的理解与灵活应用.

练习册系列答案
相关题目
7.下列氯化物中,不能通过单质之间的反应直接制取的是( )
| A. | AlCl3 | B. | FeCl3 | C. | FeCl2 | D. | CuCl2 |
11.用酸性氢氧燃料电池为电源进行电解的实验装置示意图如图所示.下列说法中正确的是( )
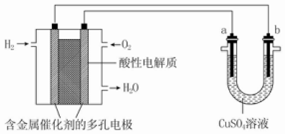

| A. | 燃料电池工作时,正极反应为 O2+2H2O+4e═4OH | |
| B. | a 极是铁,b 极是铜时,b 极逐渐溶解,a 极上有铜析出 | |
| C. | a 极是粗铜,b 极是纯铜时,a 极逐渐溶解,b 极上有铜析出 | |
| D. | a、b 两极均是石墨时,在相同条件下 a 极产生的气体与电池中消耗的 H2 体积相等 |
15.下列物质的水溶液能导电,但属于非电解质的是( )
| A. | SO2 | B. | Cl2 | C. | Na2CO3 | D. | CH3COOH |
9.(1)次磷酸(H3PO2)是一种一元中强酸,重要的精细化工产品.
①写出次磷酸的电离方程式:H3PO2?H++H2PO2-.
②已知某温度下0.01mol/L的NaOH溶液pH=10,将该NaOH溶液与等浓度等体积的H3PO2溶液混合,混合后溶液pH=7,则此时c(OH-)-c(H3PO2)=10-7mol/L.(用具体数值表示)
(2)常温下,浓度均为0.1mol•L-1的下列五种钠盐溶液的pH如表,
上述盐溶液中的阴离子,结合H+能力最强的是CO32-.根据表中数据,浓度均为0.01mol•L-1的下列四种酸的溶液分别稀释100倍,PH变化最大的是C(填编号).
A.HCN B.HClO C.CH3COOH D.H2CO3.
①写出次磷酸的电离方程式:H3PO2?H++H2PO2-.
②已知某温度下0.01mol/L的NaOH溶液pH=10,将该NaOH溶液与等浓度等体积的H3PO2溶液混合,混合后溶液pH=7,则此时c(OH-)-c(H3PO2)=10-7mol/L.(用具体数值表示)
(2)常温下,浓度均为0.1mol•L-1的下列五种钠盐溶液的pH如表,
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| PH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
A.HCN B.HClO C.CH3COOH D.H2CO3.
10.下列操作与实验现象不匹配的是( )
| 反应 | 现象 | |
| A | 把明矾溶液滴入含悬浮泥沙的水中 | 产生不溶物 |
| B | 在氯气中点燃氢气 | 产生苍白色火焰 |
| C | 将氯气通入紫色石蕊溶液 | 溶液最终由紫色变为红色 |
| D | 向硅酸钠浓溶液中滴入稀硫酸 | 出现胶状物 |
| A. | A | B. | B | C. | C | D. | D |