题目内容
最近,意大利科学家使用普通氧分子和带正电荷的氧离子制造出了由4个氧原子构成的氧分子O4,并用质谱仪探测到了它存在的证据.下列说法正确的是( )
| A、O4是氧元素的一种同位素 |
| B、O4可能含有极性键 |
| C、同温同压下,等体积的O4气体和O2含有相同的分子数 |
| D、O4转化O2为物理变化 |
考点:同素异形体,氧族元素简介
专题:氧族元素
分析:A.同位素研究对象是核素;
B.相同原子间形成的化学键是非极性共价键;
C.同温同压下,Vm相同;
D.物理变化与化学变化的本质区别是否有新物质的生成.
B.相同原子间形成的化学键是非极性共价键;
C.同温同压下,Vm相同;
D.物理变化与化学变化的本质区别是否有新物质的生成.
解答:
解:A.质子数相同中子数不同的核素互称为同位素,O4是单质,故A错误;
B.O4 中氧原子和氧原子间形成的是非极性共价键,故B错误;
C.O4和O2都是气体,同温同压条件下,Vm相同,则相同体积的任何气体具有相同的分子数,故C正确;
D.O4和O2不是同种物质,所以O4转化O2为化学变化,故D错误;
故选C.
B.O4 中氧原子和氧原子间形成的是非极性共价键,故B错误;
C.O4和O2都是气体,同温同压条件下,Vm相同,则相同体积的任何气体具有相同的分子数,故C正确;
D.O4和O2不是同种物质,所以O4转化O2为化学变化,故D错误;
故选C.
点评:本题考查了同位素,键的极性的判断,化学变化和物理变化区别,属于对基础知识的考查,题目难度不大.

练习册系列答案
相关题目
 如图装置中X和Y均为石墨电极,电解液为500mL某蓝色溶液,电解一段时间,观察到X电极表面有红色的固态物质生成,Y电极有无色气体生成;溶液中原有溶质完全电解后,停止电解,取出X电极,洗涤、干燥、称量,电极增重1.6g.下列有关说法中不正确的是( )
如图装置中X和Y均为石墨电极,电解液为500mL某蓝色溶液,电解一段时间,观察到X电极表面有红色的固态物质生成,Y电极有无色气体生成;溶液中原有溶质完全电解后,停止电解,取出X电极,洗涤、干燥、称量,电极增重1.6g.下列有关说法中不正确的是( )| A、X电极是阴极 |
| B、Y电极产生气体的体积为0.224L |
| C、电解后溶液的pH=1 |
| D、要使电解后溶液恢复到电解前的状态,需加入一定量的CuO或CuCO3 |
常温下,取0.2mol/L HX溶液与0.2mol/L NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,则下列说法(或关系式)正确的是( )
| A、c(Na+)-c(X-)=9.9×10-7mol/L |
| B、c(Na+)=c(X-)+c(HX)=0.1mol/L |
| C、c(OH-)-c(HX)=c(H+)=1×10-6mol/L |
| D、混合溶液中由水电离出的c(OH-)小于0.2mol/LHX溶液中由水电离出的c(H+) |
在25℃时两种酸的电离常数如下:H2CO3:Ki1=4.2×10-7,Ki2=5.6×10-11;H2S:Ki1=5.7×10-8,Ki2=1.2×10-15,则下列反应可能发生的是( )
| A、NaHCO3+NaHS→Na2CO3+H2S↑ |
| B、H2S+Na2CO3→NaHS+NaHCO3 |
| C、Na2S+H2O+CO2→Na2CO3+H2S↑ |
| D、H2S+NaHCO3→NaHS+H2CO3 |
关于常温下pH=12的NaOH溶液,下列说法正确的是( )
| A、c(OH-)>c(Na+)+c(H+) |
| B、由水电离出的c(OH-)=1.0×10-12mol?L-1 |
| C、与等体积pH=2的醋酸混合后所得溶液显碱性 |
| D、与等体积0.01mol?L-1氯化铵溶液混合后所得溶液中:c(Na+)=c(NH4+) |
下列各组物质中,当总物质的量一定时,不论按何种比例混合,充分燃烧后,生成水的质量为一常量,且生成CO2质量也为一定值的是( )
| A、乙烷、乙醇、乙二醇 |
| B、苯、苯酚、苯乙烯 |
| C、甲醛、乙酸、甲酸甲酯 |
| D、甲烷、乙烯、乙烷 |
 某化学实验室需要0.2mol/L NaOH溶液500mL和0.5mol/L硫酸溶液450mL.根据这两种溶液的配制情况回答下列问题:
某化学实验室需要0.2mol/L NaOH溶液500mL和0.5mol/L硫酸溶液450mL.根据这两种溶液的配制情况回答下列问题: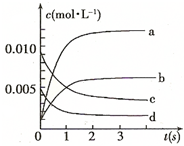 (14分)在2L密闭容器内,800℃时反应:2NO(g)+O2(g)═2NO2(g)体系中,n(NO)随时间的变化如表:
(14分)在2L密闭容器内,800℃时反应:2NO(g)+O2(g)═2NO2(g)体系中,n(NO)随时间的变化如表: