题目内容
(1)向一小烧杯中分别加入等体积的水和煤油,片刻后再向该烧杯中轻缓地加入一粒绿豆大小的金属钠,观察到的现象正确的是

(2)金属钠失火时,应该用 灭火.
(3)过氧化钠可用作潜水艇的供养剂,主要化学反应方程式为 .
(4)实验室盛放氢氧化钠溶液的试剂瓶不用玻璃塞,是因为玻璃中含 (填化学式),刻蚀玻璃常用的试剂是氢氟酸,发生反应的化学方程式为
(5)制取水泥和陶瓷的共同原料是 .

(2)金属钠失火时,应该用
(3)过氧化钠可用作潜水艇的供养剂,主要化学反应方程式为
(4)实验室盛放氢氧化钠溶液的试剂瓶不用玻璃塞,是因为玻璃中含
(5)制取水泥和陶瓷的共同原料是
考点:钠的化学性质,钠的重要化合物
专题:金属概论与碱元素
分析:(1)根据钠的化学性质、钠的密度、水和煤油的密度大小来分析;
(2)金属钠是一种活泼金属,用来灭火的物质和金属钠以及钠燃烧后的产物过氧化钠之间不能反应;
(3)过氧化钠与二氧化碳反应生成碳酸钠和氧气;
(4)实验室盛放氢氧化钠溶液的试剂瓶不能用玻璃塞,其原因是在常温下,氢氧化钠与玻璃中的二氧化硅缓慢地发生反应;玻璃的主要成分为硅酸钠、二氧化硅,HF酸可以和二氧化硅反应;
(5)粘土具有独特的可塑性与结合性,即成型性能与烧成性能,是制水泥和陶瓷时都需要用的原料;
(2)金属钠是一种活泼金属,用来灭火的物质和金属钠以及钠燃烧后的产物过氧化钠之间不能反应;
(3)过氧化钠与二氧化碳反应生成碳酸钠和氧气;
(4)实验室盛放氢氧化钠溶液的试剂瓶不能用玻璃塞,其原因是在常温下,氢氧化钠与玻璃中的二氧化硅缓慢地发生反应;玻璃的主要成分为硅酸钠、二氧化硅,HF酸可以和二氧化硅反应;
(5)粘土具有独特的可塑性与结合性,即成型性能与烧成性能,是制水泥和陶瓷时都需要用的原料;
解答:
解:(1)因钠的密度比水小,比煤油大,因此介于两者之间,在与水反应生成气体后被气体带离水层,进入煤油层后停止反应又下沉,如此往复,直至钠反应完;
故选D;
(2)沙子不易燃,能将金属钠和空气隔离,且不与燃烧的产物反应,起到灭火的作用;
故答案为:砂子;
(3)Na2O2在潜水艇中作为提供氧气的来源,反应原理为过氧化钠与二氧化碳反应生成碳酸钠和氧气,反应的化学方程式为:2Na2O2+2CO2═2Na2CO3+O2,
故答案为:2Na2O2+2CO2═2Na2CO3+O2;
(4)实验室盛放氢氧化钠溶液的试剂瓶不能用玻璃塞,其原因是在常温下,氢氧化钠与玻璃中的二氧化硅缓慢地发生反应;HF酸可以和玻璃的成分中的二氧化硅反应,可以用HF酸来刻蚀玻璃,即SiO2+4HF═SiF4↑+2H2O,
故答案为:SiO2;SiO2+4HF═SiF4↑+2H2O;
(5)生产水泥以粘土和石灰石为主要原料,经研磨、混合后在水泥回转窑中煅烧,再加入适量石膏,并研成细粉就得到普通水泥;
陶瓷的原料是粘土,经过混合、成型、干燥、烧结而成,所以制水泥和陶瓷时都需要用的原料是粘土,
故答案为:黏土;
故选D;
(2)沙子不易燃,能将金属钠和空气隔离,且不与燃烧的产物反应,起到灭火的作用;
故答案为:砂子;
(3)Na2O2在潜水艇中作为提供氧气的来源,反应原理为过氧化钠与二氧化碳反应生成碳酸钠和氧气,反应的化学方程式为:2Na2O2+2CO2═2Na2CO3+O2,
故答案为:2Na2O2+2CO2═2Na2CO3+O2;
(4)实验室盛放氢氧化钠溶液的试剂瓶不能用玻璃塞,其原因是在常温下,氢氧化钠与玻璃中的二氧化硅缓慢地发生反应;HF酸可以和玻璃的成分中的二氧化硅反应,可以用HF酸来刻蚀玻璃,即SiO2+4HF═SiF4↑+2H2O,
故答案为:SiO2;SiO2+4HF═SiF4↑+2H2O;
(5)生产水泥以粘土和石灰石为主要原料,经研磨、混合后在水泥回转窑中煅烧,再加入适量石膏,并研成细粉就得到普通水泥;
陶瓷的原料是粘土,经过混合、成型、干燥、烧结而成,所以制水泥和陶瓷时都需要用的原料是粘土,
故答案为:黏土;
点评:本题主要考查了物质的性质以及硅酸盐工业,难度不大,注意知识的积累.

练习册系列答案
相关题目
下列说法正确的是( )
| A、酸、碱、盐都是电解质 |
| B、电解质都是易溶于水的物质 |
| C、氧化物都是电解质 |
| D、氢化物都不是电解质 |
某无色溶液中存在大量的NH4+、H+、Clˉ,该溶液中还可能大量存在的离子是( )
| A、CO32ˉ |
| B、OHˉ |
| C、Cu2+ |
| D、Al3+ |
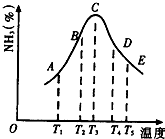 (1)在容积不同的密闭容器内,分别充入同量的N2和H2,在不同温度下,任其发生反应N2+3H2?2NH3,并分别在t秒时测定其中NH3的体积分数,绘图如图所示:
(1)在容积不同的密闭容器内,分别充入同量的N2和H2,在不同温度下,任其发生反应N2+3H2?2NH3,并分别在t秒时测定其中NH3的体积分数,绘图如图所示: