题目内容
11.能正确表示下列反应的离子方程式是( )| A. | 将磁性氧化铁溶于稀硫酸:Fe3O4+8H+=3Fe3++4H2O | |
| B. | 0.2mol明矾与300mL1mol/L的氢氧化钡溶液混合:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ | |
| C. | 将氯化亚铁溶液和稀硝酸混合:Fe2++4H++NO3-=Fe3++2H2O+NO↑ | |
| D. | 将铁粉加入稀硫酸中:2Fe+6H+=2Fe3++3H2↑ |
分析 A.磁性氧化铁为四氧化三铁,溶于稀硫酸后生成铁离子和亚铁离子;
B.二者反应生成氢氧化铝和硫酸钡;
C.得失电子不守恒;
D.不符合反应客观事实.
解答 解:A.将磁性氧化铁溶于盐酸,反应生成氯化铁、氯化亚铁,正确的离子方程式为:Fe3O4+8H+═2Fe3++Fe2++4H2O,故A错误;
B.0.2mol明矾与300mL1mol/L的氢氧化钡溶液混合,离子方程式:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓,故B正确;
C.将氯化亚铁溶液和稀硝酸混合,反应生成铁离子和一氧化氮气体,反应的离子方程式为:3Fe2++4H++NO3-═3Fe3++2H2O+NO↑,故C错误;
D.将铁粉加入稀硫酸中,离子方程式:Fe+2H+=Fe2++H2↑,故D错误;
故选:B.
点评 本题考查了离子方程式的正误判断,为高考中的高频题,明确物质的性质及发生反应的实质是解题关键,题目难度不大.

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
1.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 11.2 L Cl2与4.25 g NH3所含有的原子数一定相等 | |
| B. | 标准状况下36 g H2O与1.204×1024个O2分子所占的体积 | |
| C. | 100 mL 0.1 mol/L AlCl3溶液中,Al3+个数为0.01NA | |
| D. | 0.1 mol NH${\;}_{2}^{-}$所含电子数约为6.02×1023个 |
2.不粘锅的内壁有一薄层为聚四氟乙烯的涂层,用不粘锅烹烧饭菜时,不易粘锅烧焦.干、洗店常用有机溶剂洗衣服,目前使用的标准干洗剂的主要成份是四氯乙烯.关于聚四氟乙烯和四氯乙烯的叙述,正确的是( )
| A. | 它们都属于混合物 | B. | 它们都是乙烯的同系物 | ||
| C. | 它们的分子都不含氢原子 | D. | 聚四氟乙烯分子中含有双键 |
19.下列有关化学用语表示和概念判断叙述正确的是( )
| A. | 氢氧根离子的电子式: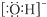 | |
| B. | 氯原子的结构示意图: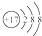 | |
| C. |  和 和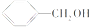 互为同系物 互为同系物 | |
| D. | SO2、NH3的水溶液能导电,故都属于电解质 |
6.下列关于金属冶炼说法正确的是 ( )
| A. | 电解铝时阴极材料需要定期更换 | |
| B. | 炼钢中添加硅、锰、铝等作为脱氧剂,调整钢水的成分,制成多种性能优良的钢材 | |
| C. | 炼钢主要目的是在高温下用还原剂将过多的碳和其他杂质还原成气体或炉渣除去 | |
| D. | 工业上一般以铁矿石、焦炭、石灰石和空气等原料在高炉中冶炼生铁 |
16.关于胶体和溶液的叙述中正确的是( )
| A. | 胶体与溶液的本质区别是能否发生丁达尔效应 | |
| B. | 胶体加入某些盐可产生沉淀,而溶液不能 | |
| C. | 胶体是一种介稳性的分散系,而溶液是一种非常稳定的分散系 | |
| D. | 胶体能够发生丁达尔现象,溶液也能发生丁达尔现象 |