题目内容
下列说法正确的是( )
| A、用湿润的碘化钾淀粉试纸检验氯化氢气体中是否混有氯气 |
| B、次氯酸具有酸性,可与碳酸钠反应产生二氧化碳气体 |
| C、新制氯水的酸性一定比久置的氯水强 |
| D、干燥氯气能使有色布条褪色 |
考点:氯气的化学性质,物质的检验和鉴别的基本方法选择及应用
专题:
分析:A、氯气与KI反应生成碘单质,遇淀粉变蓝;
B、次氯酸的酸性比碳酸的弱,弱酸不能获得强酸;
C、久置的氯水实际是稀盐酸;
D、氯气和水反应生成的次氯酸具有漂白性,但是氯气不具有.
B、次氯酸的酸性比碳酸的弱,弱酸不能获得强酸;
C、久置的氯水实际是稀盐酸;
D、氯气和水反应生成的次氯酸具有漂白性,但是氯气不具有.
解答:
解:A、氯气与KI反应生成碘单质,遇淀粉变蓝,但是氯化氢不具有该性质,则可以用湿润的碘化钾淀粉试纸检验氯化氢气体中是否混有氯气,故A正确;
B、次氯酸具有酸性,酸性比碳酸的弱,不能与碳酸钠反应产生二氧化碳气体,故B错误;
C、久置的氯水实际是稀盐酸,新制氯水的酸性比久置的氯水弱,故C错误;
D、干燥氯气不能使有色褪色,故D错误.
故选A.
B、次氯酸具有酸性,酸性比碳酸的弱,不能与碳酸钠反应产生二氧化碳气体,故B错误;
C、久置的氯水实际是稀盐酸,新制氯水的酸性比久置的氯水弱,故C错误;
D、干燥氯气不能使有色褪色,故D错误.
故选A.
点评:本题涉及氯气、氯水的性质,注意知识的迁移和应用是关键,难度不大.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
下列说法正确的是( )
| A、常温下0.4 mol/L HB溶液和0.2 mol/L NaOH溶液等体积混合后溶液的pH=3,则混合溶液中离子浓度的大小顺序为:c(Na+)>c(B-)>c(H+)>c(OH-) |
| B、常温时,pH=2的CH3COOH溶液和HCl溶液、pH=12的氨水和NaOH溶液,四种溶液中由水电离的c(H+)不相等 |
| C、pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色 |
| D、0.lmol/L pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-) |
2011年为国际化学年,主题为“化学-我们的生活,我们的未来”.下列说法不正确的是( )
| A、煤油可由石油分馏获得,可用作燃料和保存少量金属钠 |
| B、绿色化学的核心是应用化学原理对环境污染进行治理 |
| C、工业上冶炼Al,使用Al2O3而不使用AlCl3,是因为AlCl3是共价化合物,熔融不导电 |
| D、二氧化硫可用于漂白纸浆、毛、丝等,还可用于杀菌消毒 |
有Na2SO4、Fe2(SO4)3和NaNO3的混合溶液,已知其中Fe3+的物质的量浓度为0.4mol/L,SO42-的物质的量浓度为0.7mol/L,NO3-的物质的量浓度为0.2mol/L,则此溶液中Na+的物质的量浓度为(不考虑Fe3+在溶液中的反应)( )
| A、0.2mol/L |
| B、0.3mol/L |
| C、0.4mol/L |
| D、0.35mol/L |
下列物质的水溶液中,呈碱性的是( )
| A、CH3COONa |
| B、Na2SO4 |
| C、NH4Cl |
| D、KAl (SO4)2 |
如果1g水中含有m个氢原子,则阿伏加德罗常数是( )mol-1.
A、
| ||
| B、9m | ||
| C、2m | ||
| D、18m |
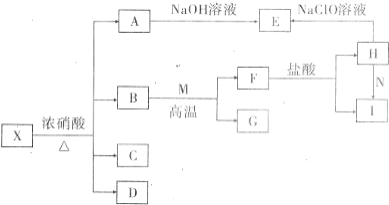 固体X是由两种常见元素组成的化合物.其中金属元素与另一元素的质量比为14:1.在一定条件下X可发生如下转化(部分产物未标出).C是无色无昧且能使澄清石灰水变浑浊的气体,D为红棕色气体,E为红褐色沉淀,M为常见金属单质.
固体X是由两种常见元素组成的化合物.其中金属元素与另一元素的质量比为14:1.在一定条件下X可发生如下转化(部分产物未标出).C是无色无昧且能使澄清石灰水变浑浊的气体,D为红棕色气体,E为红褐色沉淀,M为常见金属单质.