题目内容
60年代美国化学家鲍林提出了一个经验规则:设含氧酸的化学式为HnROm,其中(m-n)为非羟基氧原子数,鲍林认为含氧酸的强弱与非羟基氧原子数(m-n)的关系见表.
试回答下列问题:
(1)按此规则判断H3AsO4、H2CrO4、HMnO4酸性由弱到强的顺序为 .
(2)H3PO3和H3AsO3的形式一样,但酸性强弱相差很大.已知H3PO3为中强酸,H3AsO3
为弱酸,试推断H3PO3和H3AsO3的分子结构 .
(3)按此规则判断碳酸应属于 酸,与通常认为的碳酸的强度是否一致? .其可能的原因是 .
| m-n | 0 | 1 | 2 | 3 |
| 含氧酸强度 | 弱酸 | 中强 | 强 | 很强 |
| 实例 | HClO | H3PO4 | HNO3 | HClO4 |
(1)按此规则判断H3AsO4、H2CrO4、HMnO4酸性由弱到强的顺序为
(2)H3PO3和H3AsO3的形式一样,但酸性强弱相差很大.已知H3PO3为中强酸,H3AsO3
为弱酸,试推断H3PO3和H3AsO3的分子结构
(3)按此规则判断碳酸应属于
考点:判断简单分子或离子的构型,元素周期律的作用
专题:元素周期律与元素周期表专题,化学键与晶体结构
分析:(1)根据题中非羟基氧原子数与酸性强弱的关系分析;
(2)H3PO3和H3AsO3的酸性不同,说明二者分子中非羟基氧原子数不同,据此分析;
(3)根据碳酸中非羟基氧原子数判断,二氧化碳在水中溶解度不大,二氧化碳与水的反应是可逆反应.
(2)H3PO3和H3AsO3的酸性不同,说明二者分子中非羟基氧原子数不同,据此分析;
(3)根据碳酸中非羟基氧原子数判断,二氧化碳在水中溶解度不大,二氧化碳与水的反应是可逆反应.
解答:
解:(1)根据题中表格数据可知,非羟基氧原子数越多,酸性越强,
H3AsO4非羟基氧原子数为1,H2CrO4非羟基氧原子数为2,HMnO4非羟基氧原子数为3,则酸性:H3AsO4<H2CrO4<HMnO4,
故答案为:H3AsO4<H2CrO4<HMnO4;
(2)因为酸性H3PO3>H3AsO3,则H3PO3中非羟基氧的数目应大于H3AsO3,且H3AsO3为弱酸,所以可以推知H3AsO3没有非羟基氧,其分子结构分别为: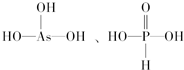 ;
;
故答案为: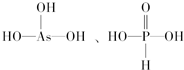 ;
;
(3)H2CO3中非羟基氧数目为1,应为中强酸,与通常认为碳酸是弱酸不一致;二氧化碳在水中溶解度不大,二氧化碳与水的反应是可逆反应,所以碳酸为弱酸其可能原因是由于溶于水的那部分CO2并不能完全转化为H2CO3;
故答案为:中强;不一致;溶于水的那部分CO2并不能完全转化为H2CO3.
H3AsO4非羟基氧原子数为1,H2CrO4非羟基氧原子数为2,HMnO4非羟基氧原子数为3,则酸性:H3AsO4<H2CrO4<HMnO4,
故答案为:H3AsO4<H2CrO4<HMnO4;
(2)因为酸性H3PO3>H3AsO3,则H3PO3中非羟基氧的数目应大于H3AsO3,且H3AsO3为弱酸,所以可以推知H3AsO3没有非羟基氧,其分子结构分别为:
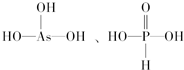 ;
;故答案为:
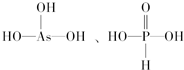 ;
;(3)H2CO3中非羟基氧数目为1,应为中强酸,与通常认为碳酸是弱酸不一致;二氧化碳在水中溶解度不大,二氧化碳与水的反应是可逆反应,所以碳酸为弱酸其可能原因是由于溶于水的那部分CO2并不能完全转化为H2CO3;
故答案为:中强;不一致;溶于水的那部分CO2并不能完全转化为H2CO3.
点评:本题考查了含有酸酸性的比较,注意对题中信息的提取和应用,明确含氧酸强弱的判断方法即可解答,题目难度中等.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
下列叙述错误的是( )
| A、NH4Cl溶液可用于去除铁锈 |
| B、用硫酸清洗锅中的水垢(主要成分为Mg(OH)2和CaCO3) |
| C、将直径为10-9~10-7m的颗粒均匀分散于水中形成的体系具有丁达尔现象 |
| D、实验室从海带中提取碘的方法是:取样→灼烧→溶解→过滤→氧化→萃取→… |
下列离子方程式错误的是( )
| A、Fe(OH)2溶液中加入HNO3溶液:Fe(OH)2+2H+═2H2O+Fe2+ |
| B、盐酸除去铜器表面的铜绿:Cu2(OH)2CO3+4H+═3H2O+2Cu2++CO2↑ |
| C、氯气可以降低的SO2的漂白性:SO2+Cl2+2H2O═2Cl-+4H++SO42- |
| D、CO2通入饱和碳酸钠溶液:CO2+CO32-+2Na++H2O═2NaHCO3↓ |
以石墨棒作电极,电解氯化铜溶液,若电解时转移的电子数是1.505×1023,则此时在阴极上析出铜的质量是( )
| A、8g | B、16g |
| C、32g | D、64g |
 反应N2O4(g)?2NO2(g)△H=+57kJ?mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
反应N2O4(g)?2NO2(g)△H=+57kJ?mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )| A、A、C两点的反应速率:A>C |
| B、A、C两点气体的颜色:A深,C浅 |
| C、由状态B到状态A,可以用加热的方法 |
| D、A、C两点气体的转化率:A>C |
 如图是短周期元素组成的非金属单质A、B、C、D,其中B、C、D在常温常压下是气体,其化合物的转化关系图(有关反应的条件及生成的H2O已略去),E是形成酸雨的污染物之一,F是常见的四原子10电子分子,化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得.化合物J由两种元素组成,其相对分子质量为32.
如图是短周期元素组成的非金属单质A、B、C、D,其中B、C、D在常温常压下是气体,其化合物的转化关系图(有关反应的条件及生成的H2O已略去),E是形成酸雨的污染物之一,F是常见的四原子10电子分子,化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得.化合物J由两种元素组成,其相对分子质量为32.
