题目内容
7.下列物质中不属于离子化合物的是( )| A. | NaOH | B. | HCl | C. | Na2O2 | D. | NH4Cl |
分析 含有离子键的化合物是离子化合物,离子化合物中可能含有共价键,一般来说,活泼金属和活泼非金属元素之间易形成离子键.
解答 解:A.NaOH中钠离子和氢氧根离子之间只存在离子键,为离子化合物,故A错误;
B.氯化氢分子中H原子和氯原子之间存在共价键,为共价化合物,故B正确;
C.Na2O2中钠离子和过氧根离子之间存在离子键为离子化合物,故C错误;
D.氯化铵中铵根离子和氯离子之间存在离子键、H原子和N原子之间存在共价键,为离子化合物,故D错误;
故选B.
点评 本题考查了化合物和化学键的关系,明确基本概念是解本题关键,根据化合物中存在的化学键确定化合物类型,题目难度不大.

练习册系列答案
 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
14.下列实验中,分离和除杂所选试剂和方法均正确的是( )
| 选项 | 目的 | 试剂 | 方法 |
| A | 分离碘水中的碘 | 乙醇 | 萃取 |
| B | 分离乙酸乙酯和乙醇 | 氢氧化钠溶液 | 分液 |
| C | 除去乙醇中乙酸 | 氧化钙 | 蒸馏 |
| D | 除去乙烷中的乙烯 | 溴的四氯化碳溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
15.常温下,下列各组离子在溶液一定能大量共存的是( )
| A. | I-Fe3+ Na+ | B. | Al3+Ba2+HCO3- | C. | K+Na+CO32- | D. | NH4+K+OH- |
15.对于平衡体系2SO2(g)+O2(g)?2SO3(g)△H<0.下列结论中正确的是( )
| A. | 若温度不变,将容器的体积增大一倍,此时的SO2浓度变为原来的0.5倍 | |
| B. | 若平衡时SO2、O2的转化率相等,说明反应开始时,两者的物质的量这比为2:1 | |
| C. | 若从平衡体系中分离出SO3,则有利于提高SO2的转化率和加快正反应速率 | |
| D. | 平衡状态时SO2、O2、SO3的物质的量之比一定为2:1:2 |
2.某有机物的结构简式为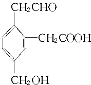 ,该有机化合物属于( )
,该有机化合物属于( )
①芳香烃 ②芳香族化合物 ③醇④羧酸 ⑤酯 ⑥醛 ⑦烃的衍生物⑧不饱和有机物⑨多官能团有机物.
 ,该有机化合物属于( )
,该有机化合物属于( )①芳香烃 ②芳香族化合物 ③醇④羧酸 ⑤酯 ⑥醛 ⑦烃的衍生物⑧不饱和有机物⑨多官能团有机物.
| A. | ②③④ | B. | ①③⑤⑥ | C. | ①③④⑤⑥⑦ | D. | ②③④⑥⑦⑧⑨ |
12.化学与生活、社会密切相关,下列说法正确的是( )
| A. | 生铁在潮湿的空气中易发生化学腐蚀而锈蚀 | |
| B. | 海水淡化能解决淡水供应危机,向海水中加净水剂明矾可以使海水淡化 | |
| C. | 在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 | |
| D. | 在米汤中加入食盐,可以检验食盐中是否加碘 |
19.已知  ,如果要合成
,如果要合成 所用的原始原料可以是( )
所用的原始原料可以是( )
 ,如果要合成
,如果要合成 所用的原始原料可以是( )
所用的原始原料可以是( )| A. | 2,3-二甲基-1,3-丁二烯和1-丁炔 | B. | 2-甲基-1,3-丁二烯和2-丁炔 | ||
| C. | 2,3-二甲基-1,3-戊二烯和乙炔 | D. | 2-甲基-1,3-丁二烯和丙炔 |
17.不能用来鉴别甲烷和乙烯的是( )
| A. | 水 | B. | 溴水 | ||
| C. | 溴的四氯化碳溶液 | D. | 酸性高锰酸钾溶液 |
