题目内容
下列各种说法正确的是( )
| A、强碱性溶液中:K+、Al3+、HCO3-、SO42-能大量共存 |
| B、室温下,pH=0的溶液中:Na+、Fe3+、NO3-、SO42-能大量共存 |
| C、0.1mol?L-1 Na2S溶液在中:c(Na+)=c(S2-)+c(HS-)+c(H2S) |
| D、0.1mol/L NaHCO3溶液中:c(Na+)>c(HCO3-)>c(OH-)>c(H+) |
考点:离子共存问题,盐类水解的应用
专题:离子反应专题,电离平衡与溶液的pH专题
分析:A.强碱性溶液,含大量的OH-;
B.pH=0的溶液,显酸性;
C.由原子守恒可知,n(Na)=2n(S);
D.碳酸氢根离子水解显碱性,且水解的程度不大.
B.pH=0的溶液,显酸性;
C.由原子守恒可知,n(Na)=2n(S);
D.碳酸氢根离子水解显碱性,且水解的程度不大.
解答:
解:A.强碱性溶液,含大量的OH-,不能大量存在Al3+、HCO3-,且Al3+、HCO3-相互促进水解,故A错误;
B.pH=0的溶液,显酸性,该组离子之间不反应,可大量共存,故B正确;
C.由原子守恒可知,n(Na)=2n(S),则
c(Na+)=c(S2-)+c(HS-)+c(H2S),故C错误;
D.碳酸氢根离子水解显碱性,c(OH-)>c(H+),且水解的程度不大,则c(Na+)>c(HCO3-)>c(OH-)>c(H+),故D正确;
故选BD.
B.pH=0的溶液,显酸性,该组离子之间不反应,可大量共存,故B正确;
C.由原子守恒可知,n(Na)=2n(S),则
| 1 |
| 2 |
D.碳酸氢根离子水解显碱性,c(OH-)>c(H+),且水解的程度不大,则c(Na+)>c(HCO3-)>c(OH-)>c(H+),故D正确;
故选BD.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重水解反应的离子共存及离子浓度大小比较的考查,题目难度不大.

练习册系列答案
相关题目
Mg、Cu和Al三种金属粉末的混合物,加入过量盐酸充分反应,过滤后向滤液中加入过量NaOH溶液,再过滤,滤液中存在的离子有( )
| A、AlO2- |
| B、Al3+ |
| C、Mg2+ |
| D、Cu2+ |
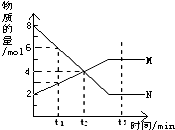 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )| A、反应的化学方程式为:2N?M |
| B、Bt2时,正逆反应速率相等,达到平衡 |
| C、t1时,N的浓度是M的浓度的2倍 |
| D、t3时,正反应速率大于逆反应速率 |
下列电解质溶液的有关叙述正确的是( )
| A、在CH3COONa溶液中加入适量CH3COOH,可使c(Na+)=c(CH3COO-) |
| B、pH=3的CH3COOH与pH=11的NaOH溶液等体积混合后,溶液显碱性 |
| C、将足量CuSO4溶液在0.1mol?L-1的H2S溶液中,Cu2+能达到的最大浓度为1.3×10-35mol?L-1(已知:Ksp(CuS)=1.3×10-36) |
| D、含1molKOH的溶液与1molCO2完全反应后,溶液中c(K+)=c(HCO3-) |