题目内容
叠氮酸钠(NaN3)是抗禽流感药物“达菲”合成过程中的中间活性物质,3molNaN3受撞击会生成4mol氮气和一种离子化合物(Na3N).下列有关叙述错误的是( )
| A、NaN3受撞击时,NaN3既是氧化剂又是还原剂 |
| B、Na3N中Na+半径比N3-半径小 |
| C、NaN3跟水反应时,有NH3生成 |
| D、NaN3中,既存在离子键又存在非极性共价键 |
考点:氧化还原反应,极性键和非极性键
专题:信息给予题
分析:由信息可知,发生3NaN3
4N2↑+Na3N,N元素的化合价既升高又降低,具有相同电子排布的离子原子序数大的离子半径小,NaN3中含离子键和N、N之间的共价键,以此来解答.
| ||
解答:
解:A.发生3NaN3
4N2↑+Na3N,N元素的化合价既升高又降低,NaN3既是氧化剂又是还原剂,故A正确;
B.Na+、N3-具有相同的电子排布,Na的原子序数大,则Na+半径比N3-半径小,故B正确;
C.Na3N与水反应生成NH3,而NaN3跟水反应时生成HN3,故C错误;
D.NaN3中,既存在Na+、N3-之间的离子键,又存在N、N之间非极性共价键,故D正确;
故选C.
| ||
B.Na+、N3-具有相同的电子排布,Na的原子序数大,则Na+半径比N3-半径小,故B正确;
C.Na3N与水反应生成NH3,而NaN3跟水反应时生成HN3,故C错误;
D.NaN3中,既存在Na+、N3-之间的离子键,又存在N、N之间非极性共价键,故D正确;
故选C.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化、化学键的形成及判断、发生的反应为解答的关键,侧重分析与应用能力考查,注意选项C中从元素化合价角度分析,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在有机合成中,制得的有机物较纯净并且容易分离,故在工业生产中有机反应往往有实用价值.试判断下列有机反应在工业上有生产价值的是( )
A、 | ||
B、CH3-CH3+Cl2
| ||
C、 | ||
D、CH3COOC2H5+H2O
|
下列属于新型无机非金属材料的是( )
| A、高强度水泥 | B、钢化玻璃 |
| C、刚玉 | D、光导纤维 |
下列实验操作或装置(略去部分加持仪器)正确的是( )
A、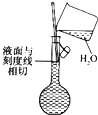 配制溶液 |
B、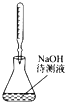 中和滴定 |
C、 制备乙酸乙酯 |
D、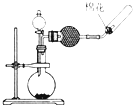 制备收集干燥的氨气 |
在一真空密闭容器中,通入一定量气体A,一定条件下,发生如下反应:2A(g)?B(g)+xC(g),反应达到平衡时,测得容器内压强增大了p%,若此时A的转化率为a%,下列关系正确的是( )
| A、若x=1,则p>a |
| B、若x=2,则p>a |
| C、若x=3,则p=a |
| D、若x=4,则p≥a |
正确掌握好化学用语是学好化学的基础.下列各选项的化学用语中正确的是( )
| A、乙烯的结构简式为CH2CH2 |
| B、乙醇的结构简式为C2H6O |
| C、丙烷的分子式为C3H8 |
D、羟基的电子式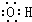 |
奥体中心体育场宛如水晶皇冠般璀璨地闪耀在浑河南岸,场馆建设中使用了大量的钢筋,下列关于钢筋的说法中不 正确的是( )
| A、钢筋是混合物 |
| B、钢筋属于金属材料 |
| C、钢筋的韧性优于生铁 |
| D、钢筋混凝土就是钢筋和混凝土的合成材料 |