题目内容
1.进行硫酸铜晶体结晶水含量的测定实验中需要进行多次加热、冷却、称量,其中称量操作至少进行( )| A. | 5次 | B. | 4次 | C. | 3次 | D. | 2次 |
分析 在硫酸铜晶体结晶水含量测定的实验中,应知道晶体的质量以及加热分解后硫酸铜固体的质量,为减小实验误差,则至少重复称量加热的操作,以此解答该题.
解答 解:在硫酸铜晶体结晶水含量测定的实验中,至少需要称量坩埚以及硫酸铜晶体结晶水的质量、灼烧后硫酸铜的质量、第二次硫酸铜的质量且与第一次质量相同,至少需要称量4次.
故选B.
点评 本题考查实验方案的评价,为高频考点,侧重考查硫酸铜结晶水的测定,既要学生分析实验的关键、细节,又要求对实验结果产生的误差的原因进行分析.既考查了学生对化学实验的基本操作和常见仪器的认识和使用,又考查了学生分析问题和解决问题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.下列仪器可以用酒精灯直接加热的是( )
| A. | 试管,烧杯 | B. | 烧瓶,烧杯 | C. | 试管,蒸发皿 | D. | 蒸发皿,量筒 |
16.为了除去粗盐中的Ca2+、Mg2+、SO42-和泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤 ②加过量的NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液,正确的操作顺序是( )
| A. | ①④②⑤③ | B. | ④①②⑤③ | C. | ②⑤④①③ | D. | ④⑤②①③ |
6.硫酸铜结晶水含量测定的实验中,若操作正确而实验测得的硫酸铜晶体中结晶水的含量偏低,其原因可能有( )
| A. | 被测样品中含有加热不挥发的杂质 | B. | 被测样品中含有加热易挥发的杂质 | ||
| C. | 实验前被测样品已有部分失水 | D. | 加热前所用的坩埚未完全干燥 |
10.氮氧化物废气是一种毒性很大的黄烟,不经治理通过烟囱排放到大气中,对生态环境和人类健康带来较大的威胁.工业生产硝酸的尾气中含有氮氧化物NOx(NO和NO2的混合物,假设不含N2O4),常见处理法有:
(1)可用氨催化吸收法处理NOx,反应原理如下:4xNH3+6NOx$\frac{\underline{\;催化剂\;}}{\;}$(2x+3)N2+6xH2O
某化学兴趣小组模拟该处理过程的实验装置如图1
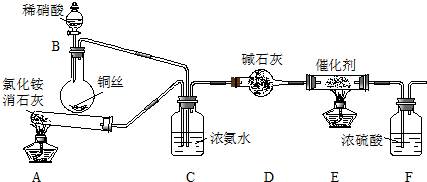
①装置A中发生反应的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
②装置D中碱石灰的作用是除去气体中含有的水蒸气.
(2)用Na2CO3溶液吸收法处理NOx.
已知:NO不能与Na2CO3溶液反应.
NO+NO2+Na2CO3═2NaNO2+CO2 (Ⅰ)
2NO2+Na2CO3═NaNO2+NaNO3+CO2 (Ⅱ)
①当NOx被Na2CO3溶液完全吸收时,x的值不可能是D(填字母).
A.1.9 B.1.7 C.1.5 D.1.3
②用足量的Na2CO3溶液完全吸收NOx,每产生22.4L(标准状况)CO2(全部逸出)时,吸收液质量就增加44g,则NOx中的x值为1.875.
(3)用固体氧化物电解池通过电解方式分解NOx.当以Pt作电极时,固体氧化物电解池还原NO示意图如图2.
298K时,有关实验数据如下,(化学反应消耗的电能占总电能的80%)
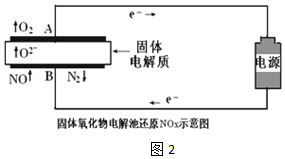
(实验所得数据均为多次平行试验的平均值)
①根据实验组1数据,NO分解的热化学方程式2NO(g)=N2(g)+O2(g)△H=+3.2akJ•mol-1
②实验组2明显比实验组1生成的N2少,其原因用电极反应式表示为O2+4e-=2O2-或2NO2+8e-=4O2-+N2.
(1)可用氨催化吸收法处理NOx,反应原理如下:4xNH3+6NOx$\frac{\underline{\;催化剂\;}}{\;}$(2x+3)N2+6xH2O
某化学兴趣小组模拟该处理过程的实验装置如图1

①装置A中发生反应的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
②装置D中碱石灰的作用是除去气体中含有的水蒸气.
(2)用Na2CO3溶液吸收法处理NOx.
已知:NO不能与Na2CO3溶液反应.
NO+NO2+Na2CO3═2NaNO2+CO2 (Ⅰ)
2NO2+Na2CO3═NaNO2+NaNO3+CO2 (Ⅱ)
①当NOx被Na2CO3溶液完全吸收时,x的值不可能是D(填字母).
A.1.9 B.1.7 C.1.5 D.1.3
②用足量的Na2CO3溶液完全吸收NOx,每产生22.4L(标准状况)CO2(全部逸出)时,吸收液质量就增加44g,则NOx中的x值为1.875.
(3)用固体氧化物电解池通过电解方式分解NOx.当以Pt作电极时,固体氧化物电解池还原NO示意图如图2.
298K时,有关实验数据如下,(化学反应消耗的电能占总电能的80%)

| 实验序号 | B极气体 | 电路中通过电子 | 消耗总电能 | 生成N2 |
| 实验1 | NO | 1mol | a KJ | 0.25mol |
| 实验2 | NO和空气 (不考虑NO2) | 1mol | a KJ | 0.09mol |
①根据实验组1数据,NO分解的热化学方程式2NO(g)=N2(g)+O2(g)△H=+3.2akJ•mol-1
②实验组2明显比实验组1生成的N2少,其原因用电极反应式表示为O2+4e-=2O2-或2NO2+8e-=4O2-+N2.
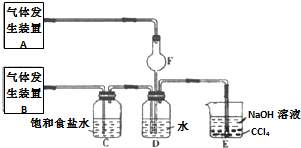
 实验室制备溴苯可用如图所示装置.填空:
实验室制备溴苯可用如图所示装置.填空: .
.
 如图为实验室制备乙烯的装置图,请回答:
如图为实验室制备乙烯的装置图,请回答: