题目内容
已知 2H2(g)+O2(g)=2H2O(L)△H=-572kJ/mol;CO(g)+
O2(g)=CO2(g)△H=-283.0kJ/mol
某H2和CO的混合气体完全燃烧时放出113.8kJ热量,同时生成3.6g液态水,则原混合气体中H2和CO的物质的量之比为多少?
| 1 |
| 2 |
某H2和CO的混合气体完全燃烧时放出113.8kJ热量,同时生成3.6g液态水,则原混合气体中H2和CO的物质的量之比为多少?
考点:有关混合物反应的计算,有关反应热的计算
专题:计算题
分析:先根据n=
计算出生成水的质量,然后利用反应2H2+O2═2H2O(l)可计算氢气的物质的量,再利用混合气体燃烧放出的热量与氢气燃烧放出的热量来计算CO燃烧放出的热量,再利用热化学反应方程式来计算CO的物质的量,最后计算出原混合气体中H2和CO的物质的量之比.
| m |
| M |
解答:
解:3.6g水的物质的量为:n(H2O)=
=0.2mol,由反应方程式2H2+O2═2H2O可知,n(H2)=n(H2O)=0.2mol,
由2H2(g)+O2(g)═2H2O(l)△H=-572kJ?mol-1可知:0.2molH2燃烧放出的热量为57.2kJ,
则CO燃烧放出的热量为:113.8KJ-57.2KJ=56.6kJ,
设混合气体中CO的物质的量为x,则
CO(g)+
O2(g)=CO2(g)△H=-283kJ?mol-1
1 283kJ
x 56.6kJ
则:x=
=0.2mol,
即原混合气体中一氧化碳的物质的量为0.20mol,
所以原混合气体中H2和CO的物质的量均为0.2mol,二者的物质的量之比为1:1,
答:则原混合气体中H2和CO的物质的量之比为1:1.
| 3.6g |
| 18g/mol |
由2H2(g)+O2(g)═2H2O(l)△H=-572kJ?mol-1可知:0.2molH2燃烧放出的热量为57.2kJ,
则CO燃烧放出的热量为:113.8KJ-57.2KJ=56.6kJ,
设混合气体中CO的物质的量为x,则
CO(g)+
| 1 |
| 2 |
1 283kJ
x 56.6kJ
则:x=
| 56.6kJ×1 |
| 283kJ |
即原混合气体中一氧化碳的物质的量为0.20mol,
所以原混合气体中H2和CO的物质的量均为0.2mol,二者的物质的量之比为1:1,
答:则原混合气体中H2和CO的物质的量之比为1:1.
点评:本题考查有关反应热的计算,题目难度中等,试题侧重基础知识的考查,明确物质的量与热量的正比例关系是解答的关键,试题有利于提高学生的分析、理解能力.

练习册系列答案
相关题目
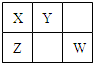 已知X、Y、Z、W四种短周期主族元素在周期表中的相对位置如图,其中X原子最外层电子数是其电子层数的2倍.下列说法正确的是( )
已知X、Y、Z、W四种短周期主族元素在周期表中的相对位置如图,其中X原子最外层电子数是其电子层数的2倍.下列说法正确的是( )| A、四种元素的原子半径大小rY>rW>rX>rZ |
| B、元素X的含氧酸只有一种,元素Y则有两种 |
| C、元素Z的气态氢化物的稳定性比元素Y的强 |
| D、元素Y和W的氧化物是导致酸雨的主要原因 |
元素周期表短周期的一部分,且M、X、Y、Z为主族元素,下列说法正确的是( )
| M | ||
| X | Y | Z |
| A、Y的氢化物的沸点一定比M的氢化物的沸点高 |
| B、Z的最高价氧化物对应的水化物有可能是弱电解质 |
| C、这四种元素形成的晶体单质都是分子晶体 |
| D、单质M的晶体中可能含有共价键和分子间作用力 |
下列说法中正确的是( )
| A、为了快速配制好溶液,可以用容量瓶直接溶解氯化钠固体来配制溶液 |
| B、Cu中混有CuO,可以通过加入足量盐酸溶液,再过滤、洗涤烘干可得到洁净的Cu |
| C、设NA为阿伏伽德罗常数的值,1.0 L c(H+)=1.0mol/L的硫酸溶液中含有的H+数为NA |
| D、Fe(OH)3胶体是能产生丁达尔效应的分散系,而CuSO4溶液和蒸馏水是不能产生丁达尔效应的分散系 |
将50mL 0.5mol/L的Al2(SO4)3溶液加入4.0mol/L NaOH溶液可得到2.34g沉淀.则消耗的NaOH溶液的体积可能是( )
| A、45ml | B、30ml |
| C、42.5ml | D、60ml |
 工业上利用电解饱和食盐水可制得重要化工产品,该工业又称为“氯碱工业”.
工业上利用电解饱和食盐水可制得重要化工产品,该工业又称为“氯碱工业”. 4.53g硫酸铝铵晶体加热分解,最终剩余0.51g Al2O3固体.加热过程中,固体质量随温度的变化如图所示.请通过计算确定400℃时剩余固体成分的化学式(写出计算过程).
4.53g硫酸铝铵晶体加热分解,最终剩余0.51g Al2O3固体.加热过程中,固体质量随温度的变化如图所示.请通过计算确定400℃时剩余固体成分的化学式(写出计算过程).