题目内容
17.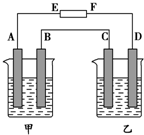 如图中,甲烧杯中盛有100mL 0.50mol•L-1 AgNO3溶液,乙烧杯中盛有100mL 0.25mol•L-1 CuCl2溶液,A、B、C、D均为质量相同的石墨电极,如果电解一段时间后,发现A极比C极重1.9g,则
如图中,甲烧杯中盛有100mL 0.50mol•L-1 AgNO3溶液,乙烧杯中盛有100mL 0.25mol•L-1 CuCl2溶液,A、B、C、D均为质量相同的石墨电极,如果电解一段时间后,发现A极比C极重1.9g,则(1)A极析出的物质0.025mol.C极析出的物质0.0125mol.
(2)B极的电极反应式为4OH--4e-═2H2O+O2↑.
分析 电解池中,发现A极比C极重1.9g,则A极是阴极,和电源的负极相连的是阴极,即E是负极,F是正极,B是阳极,C是阴极,D是阳极,
(1)A极是阴极,电极反应式为:Ag++e-=Ag,C是阴极,电极反应为:Cu2++2e-=Cu,析出金属铜,A极比C极重1.9g,设电路转移电子是x,则108x-32x=1.9,所以x=0.025mol;C是阴极,电极反应式为:Cu2++2e-=Cu,电路转移电子0.025mol,生成金属铜是0.0125mol;
(2)B是阳极,该极上是氢氧根离子失电子,电极反应为:4OH--4e-═H2O+O2↑.
解答 解:(1)A极是阴极,电极反应式为:Ag++e-=Ag,C是阴极,电极反应为:Cu2++2e-=Cu,析出金属铜,A极比C极重1.9g,设电路转移电子是x,则108x-32x=1.9,所以x=0.025mol,析出金属银的物质的量是0.025mol;C是阴极,电极反应式为:Cu2++2e-=Cu,电路转移电子0.025mol,生成金属铜是0.0125mol,
故答案为:0.025mol;0.0125;
(2)B是阳极,该极上是氢氧根离子失电子,电极反应为:4OH--4e-═H2O+O2↑,故答案为:4OH--4e-═2H2O+O2↑.
点评 本题考查学生电解池的工作原理以及离子放电顺序以及电极反应式的书写知识,难度不大,注意知识的灵活应用是关键.

练习册系列答案
相关题目
16.下图是CH4、CCl4、CH3Cl的分子球棍模型图,下列说法正确的是( )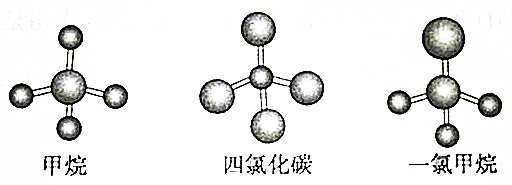

| A. | CH4、CCl4和CH3Cl都是正四面体结构 | |
| B. | CH4、CCl4都是正四面体结构 | |
| C. | CH4和CCl4中的化学键均为非极性键 | |
| D. | CH4、CCl4的结构相同,性质也相同 |
8.A.B.C是周期表中相邻的三个元素,A和B是同周期,B和C同主族,三种元素最外层电子总数之和为17,核内质子数之和为31,则A.B.C三种元素是( )
| A. | Mg、Al、B | B. | Li、Be、Mg | C. | N、O、S | D. | O、F、C |
5.以下自发进行反应可用能量判据来解释的是( )
| A. | 硝酸铵自发地溶于水 | |
| B. | 2N2O5(g)═4NO2(g)+O2(g)△H=+56.7kJ•mol-1 | |
| C. | (NH4 )2 CO3(s)═NH4HCO3(s)+NH3(g);△H=+74.9 kJ/mol | |
| D. | 2H2(g)+O2(g)═2H2O(l);△H=-571.6 KJ/mol |
12.某原电池总反应的离子方程式是Zn+Cu2+═Zn2++Cu,该原电池的正确组成是( )
| A | B | C | D | |
| 正极 | Zn | Cu | Cu | Fe |
| 负极 | Cu | Zn | Zn | Zn |
| 电解质溶液 | CuCl2 | H2SO4 | AgNO3 | CuCl2 |
| A. | A | B. | B | C. | C | D. | D |
2.在下列物质中,既含离子键又含共价键的是( )
| A. | MgCl2 | B. | KOH | C. | H2O | D. | Cl2 |
9.已知X、Y、Z三种元素的为同一周期的元素,且它们的最高价氧化物对应的水化物酸性依次增强,则下列判断不正确的是( )
| A. | 原子半径按X、Y、Z的顺序增大 | B. | 原子序数按X、Y、Z顺序增大 | ||
| C. | 单质的氧化性按X、Y、Z顺序增强 | D. | 氢化物的稳定性按X、Y、Z顺序增强 |
6.下列有关热化学方程式及其叙述正确的是( )
| A. | 氢气的燃烧热为285.5 kJ/mol,则水电解的热化学方程式为:2H2O(l)═2H2(g)+O2(g)△H=+285.5 kJ/mol | |
| B. | 1mol甲烷完全燃烧生成CO2和H2O(l)时放出890 kJ热量,它的热化学方程式为:$\frac{1}{2}$CH4(g)+O2(g)═$\frac{1}{2}$CO2(g)+H2O(l)△H=-445 kJ/mol | |
| C. | 已知2C(s)+O2(g)═2CO(g)△H=-221 kJ•mol-1,则C(S)的燃烧热为-110.5 kJ/mol | |
| D. | HF与NaOH溶液反应:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ/mol |
7.有八种物质:①甲烷、②苯、③聚乙烯、④聚异戊二烯、⑤2-丁炔、⑥环己烷、⑦环己烯,既能使酸性高锰酸钾溶液褪色,又能使溴水因反应而褪色的是( )
| A. | ③④⑤⑧ | B. | ④⑤⑦ | C. | ④⑤ | D. | ③④⑤⑦⑧ |