题目内容
20.用石墨电极电解CuSO4溶液一段时间后,向所得溶液中加入0.2mol Cu(OH)2后,恰好使溶液恢复到电解前的浓度.则电解过程中转移的电子的物质的量为( )| A. | 0.4 mol | B. | 0.5 mol | C. | 0.6 mol | D. | 0.8 mol |
分析 将Cu(OH)2改写为CuO•H2O,根据CuO•H2O知,阳极上OH-放电生成O2,阴极上Cu2+和H+放电生成Cu和H2,根据阳极上生成O2与转移电子之间的关系计算转移电子物质的量.
解答 解:Cu(OH)2改写为CuO•H2O,根据CuO•H2O知,阳极上OH-放电生成O2,阴极上Cu2+和H+放电生成Cu和H2,根据氧原子守恒得n(O2)=n[Cu(OH)2]=0.2mol,则转移电子的物质的量=0.2mol×4=0.8mol,故选D.
点评 本题以电解原理为载体考查物质的量有关计算,为高频考点,明确各个电极上放电微粒是解本题关键,注意原子守恒的灵活运用,题目难度不大.

练习册系列答案
相关题目
13.下列说法正确的是( )
| A. | 合金都一定是两种金属熔合而成 | |
| B. | 涂料属于高分子材料,不属于合成材料 | |
| C. | 水泥与水搅拌静之后会凝固变硬,这是水泥的水硬性 | |
| D. | 我国的陶都和瓷都都是宜兴 |
11.25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 能使甲基橙变红的溶液中:NH4+、Mg2+、SO42-、NO3- | |
| B. | 1.0 mol•L-1FeCl3溶液:Na+、Cl-、NO3-、SCN- | |
| C. | 1.0 mol•L-1的KNO3溶液中:Fe2+、H+、Cl-、SO42- | |
| D. | 与Al反应能放出H2的溶液中:Na+、Cl-、HCO3-、SO42- |
15.如图所示的实验,发现烧杯中酸性KMn04溶液褪色.若将烧杯中的溶液换成含有少量KSCN的FeS04溶液,溶液呈血红色.判断下列说法中不正确的是( )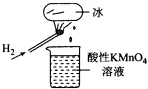

| A. | 该条件下H2燃烧生成了既具有氧化性又具有还原性的物质 | |
| B. | 该条件下H2燃烧的产物中可能含有一定量的H2O2、HO2等 | |
| C. | 将烧杯中溶液换成KI淀粉溶液也能验证生成物具有还原性 | |
| D. | 酸性FeSO4溶液中加入双氧水的离子反应为:2Fe 2++H2O2+2H+=2Fe3++2H20 |
5.分类法在化学学科的发展中起到了非常重要的作用,下列分类标准合理的是( )
| A. | 根据是否含氧元素,将物质分为氧化剂和还原剂 | |
| B. | 根据反应中是否有电子转移,将化学反应分为氧化还原反应和非氧化还原反应 | |
| C. | 根据水溶液是否能够导电,将物质分为电解质和非电解质 | |
| D. | 根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体 |
12.下列实验现象描述不正确的是( )
| 编码 | 实验 | 现象 |
| A | 加热放在坩埚中的小块钠 | 钠先融化成光亮的小球,燃烧时,火焰为黄色,燃烧后,生成淡黄色固体 |
| B | 在酒精灯上加热铝箔 | 铝箔融化,失去光泽,融化的铝并不滴落,好像一层膜兜着 |
| C | 在空气中久置的铝条放入NaOH溶液中 | 铝条立刻产生大量无色气泡,铝条逐渐变细,铝条逐渐发热 |
| D | 在FeCl2溶液中滴入NaOH溶液 | 生成白色沉淀,沉淀很快变为灰绿色,最后变为红褐色 |
| A. | A | B. | B | C. | C | D. | D |
9.根据下列四种粒子的结构示意图,所获取的信息不正确的是( )
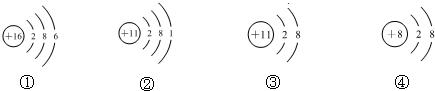
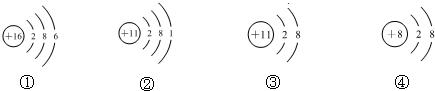
| A. | 它们表示四种元素 | |
| B. | ②③的化学性质相同 | |
| C. | ②表示的元素是金属元素 | |
| D. | ①表示的是原子,而④表示的是阴离子 |
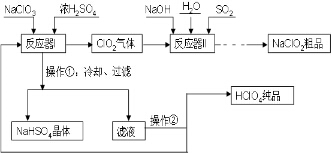 工业上生产高氯酸(沸点:90°C)时还同时生产了亚氯酸钠,其工艺流程如下:
工业上生产高氯酸(沸点:90°C)时还同时生产了亚氯酸钠,其工艺流程如下: