题目内容
(1)标准状况下,CO和CO2混合气体的质量为36g,体积为22.4L,则CO所占的体积为 L,质量为 g,混合气体中CO2的分子数为 .
(2)3.01×1023个OH-的物质的量为 ,质量为 ,它与标准状况下 L的NH3的物质的量相等,与 gNa+含有的离子数目相同.
(3)下列物质中:①HClO ②苛性钠 ③铁 ④乙醇 ⑤氨水 ⑥H2SO4 ⑦水 ⑧硫酸钡 ⑨二氧化碳
属于电解质的是(填序号,下同) ,
属于强电解质的是 ,
属于非电解质的是 ,
既不属于电解质也不属于非电解质的是 .
(2)3.01×1023个OH-的物质的量为
(3)下列物质中:①HClO ②苛性钠 ③铁 ④乙醇 ⑤氨水 ⑥H2SO4 ⑦水 ⑧硫酸钡 ⑨二氧化碳
属于电解质的是(填序号,下同)
属于强电解质的是
属于非电解质的是
既不属于电解质也不属于非电解质的是
考点:物质的量的相关计算,电解质与非电解质,强电解质和弱电解质的概念
专题:计算题,电离平衡与溶液的pH专题
分析:(1)令CO和CO2的物质的量分别为xmol、ymol,根据二者质量和体积列方程计算,再根据V=nVm计算CO的体积,根据m=nM计算CO的质量,根据N=nNA计算CO2的分子数;
(2)根据n=
计算OH-的物质的量,根据m=nM计算OH-的质量,根据V=nVm计算氨气的体积,根据m=nM计算钠离子质量;
(3)熔融状态下或水溶液中能导电的化合物是电解质,酸、碱、盐、活泼金属氧化物等都是电解质;
在水溶液中和熔融状态下都不能够导电的化合物称为非电解质,大部分有机物、非金属氧化物等是非电解质;
能全部电离的电解质是强电解质,包括强酸、强碱、大部分盐、活泼金属氧化物;
只有部分电离的电解质是弱电解质,包括弱酸、弱碱和水等;
单质和混合物既不是电解质,也不是非电解质.
(2)根据n=
| N |
| NA |
(3)熔融状态下或水溶液中能导电的化合物是电解质,酸、碱、盐、活泼金属氧化物等都是电解质;
在水溶液中和熔融状态下都不能够导电的化合物称为非电解质,大部分有机物、非金属氧化物等是非电解质;
能全部电离的电解质是强电解质,包括强酸、强碱、大部分盐、活泼金属氧化物;
只有部分电离的电解质是弱电解质,包括弱酸、弱碱和水等;
单质和混合物既不是电解质,也不是非电解质.
解答:
解:(1)令CO和CO2的物质的量分别为xmol、ymol,根据二者质量和体积列方程,则:
,解得x=y=0.5,
标况下,CO的体积=0.5mol×22.4L/mol=11.2L,CO的质量=0.5mol×28g/mol=14g,CO2的分子数=0.5mol×6.02×1023mol-1=3.01×1023mol,
故答案为:11.2;14;3.01×1023;
(2)3.01×1023个OH-的物质的量为
=0.5mol,质量为0.5mol×17g/mol=8.5g,与之物质的量相等的NH3再标况下体积=0.5mol×22.4L/mol=11.2L,与之含有相同离子数目的Na+的质量=0.5mol×23g/mol=11.5g,
故答案为:0.5mol;8.5g;11.2;11.5;
(3)①HClO在水溶液中能自身电离而导电,属于电解质,次氯酸是弱酸,属于弱电解质;
②苛性钠在水溶液或熔融状态下都能自身电离而导电,属于电解质,为强碱,属于强电解质;
③铁是单质,既不是电解质也不是非电解质;
④乙醇在水溶液和熔融状态下都不能自身电离而导电,属于非电解质;
⑤氨水为混合物,既不是电解质,也不是非电解质;
⑥硫酸在水溶液中能自身电离而导电,属于电解质,为强酸,属于强电解质;
⑦水能够微弱的导电,属于弱电解质;
⑧硫酸钡在熔融状态下能自身电离而导电,属于电解质,在溶液中完全电离,属于强电解质;
⑨二氧化碳在水溶液和熔融状态下都不能自身电离而导电,属于非电解质;
所以属于电解质的是:①②⑥⑦⑧;属于强电解质的是:②⑥⑧,属于非电解质的是:④⑨;既不属于电解质又不属于非电解质的是:③⑤,
故答案为:①②⑥⑦⑧;②⑥⑧;④⑨;③⑤.
|
标况下,CO的体积=0.5mol×22.4L/mol=11.2L,CO的质量=0.5mol×28g/mol=14g,CO2的分子数=0.5mol×6.02×1023mol-1=3.01×1023mol,
故答案为:11.2;14;3.01×1023;
(2)3.01×1023个OH-的物质的量为
| 3.01×1023 |
| 6.02×1023mol-1 |
故答案为:0.5mol;8.5g;11.2;11.5;
(3)①HClO在水溶液中能自身电离而导电,属于电解质,次氯酸是弱酸,属于弱电解质;
②苛性钠在水溶液或熔融状态下都能自身电离而导电,属于电解质,为强碱,属于强电解质;
③铁是单质,既不是电解质也不是非电解质;
④乙醇在水溶液和熔融状态下都不能自身电离而导电,属于非电解质;
⑤氨水为混合物,既不是电解质,也不是非电解质;
⑥硫酸在水溶液中能自身电离而导电,属于电解质,为强酸,属于强电解质;
⑦水能够微弱的导电,属于弱电解质;
⑧硫酸钡在熔融状态下能自身电离而导电,属于电解质,在溶液中完全电离,属于强电解质;
⑨二氧化碳在水溶液和熔融状态下都不能自身电离而导电,属于非电解质;
所以属于电解质的是:①②⑥⑦⑧;属于强电解质的是:②⑥⑧,属于非电解质的是:④⑨;既不属于电解质又不属于非电解质的是:③⑤,
故答案为:①②⑥⑦⑧;②⑥⑧;④⑨;③⑤.
点评:本题考查物质的量有关计算、电解质与非电解质等,比较基础,侧重对基础知识的巩固,注意电解质和非电解质都必须是化合物,且自身电离出自由移动的离子,单质和混合物既不是电解质也不是非电解质.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列各组物质在一定条件下反应,可以制得较纯净的氯乙烷的是( )
| A、乙烷与氯气混合 |
| B、乙烯与氯气混合 |
| C、乙烯与氯化氢气体混合 |
| D、乙烯通入浓盐酸中 |
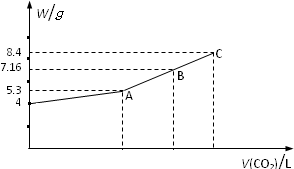 往NaOH溶液中通入CO2气体充分反应后,在低压和低温下,小心地将溶液蒸干,得到白色的固体M,通入CO2的体积V(CO2)(标准状况)与M的质量W的关系如下图.
往NaOH溶液中通入CO2气体充分反应后,在低压和低温下,小心地将溶液蒸干,得到白色的固体M,通入CO2的体积V(CO2)(标准状况)与M的质量W的关系如下图. ,可通过它用不同化学反应分别制得B、C和D 三种物质.
,可通过它用不同化学反应分别制得B、C和D 三种物质.