题目内容
某小组同学将一定浓度NaHCO3溶液加入到CuSO4溶液中发现生成了沉淀.甲同学认为沉淀是CuCO3;乙同学认为沉淀是CuCO3和Cu(OH)2的混合物,他们设计实验测定沉淀中CuCO3的质量分数.
(1)按照甲同学的观点,发生反应的离子方程式为 ;
(2)乙同学认为有Cu(OH)2生成的理论依据是 (用离子方程式表示);
(3)两同学利用如图所示装置进行测定

①在研究沉淀物组成前,须将沉淀从溶液中分离并净化.具体操作依次为 、洗涤、干燥;
②装置E中碱石灰的作用是 ;
③实验过程中有以下操作步骤:a.关闭K1、K3,打开K2、K4,充分反应; b.打开K1、K4,关闭K2、K3,通入过量空气;c.打开K1、K3,关闭K2、K4,通入过量空气.正确的顺序是 (填选项序号,下同);若未进行步骤 ,将使测量结果偏低;
④若沉淀样品的质量为m g,装置D的质量增加了n g,则沉淀中CuCO3的质量分数为 .
(1)按照甲同学的观点,发生反应的离子方程式为
(2)乙同学认为有Cu(OH)2生成的理论依据是
(3)两同学利用如图所示装置进行测定

①在研究沉淀物组成前,须将沉淀从溶液中分离并净化.具体操作依次为
②装置E中碱石灰的作用是
③实验过程中有以下操作步骤:a.关闭K1、K3,打开K2、K4,充分反应; b.打开K1、K4,关闭K2、K3,通入过量空气;c.打开K1、K3,关闭K2、K4,通入过量空气.正确的顺序是
④若沉淀样品的质量为m g,装置D的质量增加了n g,则沉淀中CuCO3的质量分数为
考点:探究物质的组成或测量物质的含量
专题:
分析:(1)按照甲同学的观点,HCO3-电离生成H+和CO32-,CO32-与Cu2+反应生成CuCO3沉淀,H+与HCO3-反应生成CO2和H2O;
(2)乙同学认为有Cu(OH)2生成的理论依据NaHCO3溶液加入到CuSO4溶液中铜离子交换碳酸氢根离子水解生成的氢氧根离子生成氢氧化铜沉淀,促进水解反应进行;
(3)①将沉淀从溶液中分离并净化,应进行过滤、洗涤和干燥等操作;
②为准确测定生成CO2的质量,应防止空气中CO2和水蒸气进入装置;
③为减小实验误差,应先通入过量经NaOH处理的空气,排除装置内的二氧化碳气体,一段时间之后,再进行实验,最后还要通入过量经NaOH处理的空气,使生成的二氧化碳全部被吸收;
④装置D的质量增加了ng,应为CO2的质量,则m(CuCO3)=
,以此计算沉淀中CuCO3的质量分数;
(2)乙同学认为有Cu(OH)2生成的理论依据NaHCO3溶液加入到CuSO4溶液中铜离子交换碳酸氢根离子水解生成的氢氧根离子生成氢氧化铜沉淀,促进水解反应进行;
(3)①将沉淀从溶液中分离并净化,应进行过滤、洗涤和干燥等操作;
②为准确测定生成CO2的质量,应防止空气中CO2和水蒸气进入装置;
③为减小实验误差,应先通入过量经NaOH处理的空气,排除装置内的二氧化碳气体,一段时间之后,再进行实验,最后还要通入过量经NaOH处理的空气,使生成的二氧化碳全部被吸收;
④装置D的质量增加了ng,应为CO2的质量,则m(CuCO3)=
| ng |
| 44g/mol |
解答:
解:(1)按照甲同学的观点,HCO3-电离生成H+和CO32-,CO32-与Cu2+反应生成CuCO3沉淀,H+与HCO3-反应生成CO2和H2O,
反应的方程式为Cu2++2HCO3-=CuCO3↓+CO2↑+H2O(或:Cu2++HCO3-=CuCO3↓+H+、H++HCO3-=CO2↑+H2O),
故答案为:Cu2++2HCO3-=CuCO3↓+CO2↑+H2O(或:Cu2++HCO3-=CuCO3↓+H+、H++HCO3-=CO2↑+H2O);
(2)乙同学认为有Cu(OH)2生成的理论依据是HCO3-+H2O?H2CO3+OH-、Cu2++2OH-=Cu(OH)2↓;
故答案为:HCO3-+H2O?H2CO3+OH-、Cu2++2OH-=Cu(OH)2↓;
(3)①将沉淀从溶液中分离并净化,应进行过滤、洗涤和干燥等操作,故答案为:过滤;
②为准确测定生成CO2的质量,应防止空气中CO2和水蒸气进入装置,
故答案为:防止空气中CO2和水蒸气进入装置D;
③为减小实验误差,应先通入过量经NaOH处理的空气,排除装置内的二氧化碳气体,即打开K1、K3,关闭K2、K4,通入过量空气,一段时间之后,再关闭K1、K3,打开K2、K4,充分反应,最后还要通入过量经NaOH处理的空气,使生成的二氧化碳全部被吸收,即打开K1、K4,关闭K2、K3,通入过量空气,如若未进行步骤b,将使测量结果偏低,
故答案为:cab; b;
④装置D的质量增加了ng,应为CO2的质量,则m(CuCO3)=
,则沉淀中CuCO3的质量分数为
×100%=
×100%,
故答案为:
×100%;
反应的方程式为Cu2++2HCO3-=CuCO3↓+CO2↑+H2O(或:Cu2++HCO3-=CuCO3↓+H+、H++HCO3-=CO2↑+H2O),
故答案为:Cu2++2HCO3-=CuCO3↓+CO2↑+H2O(或:Cu2++HCO3-=CuCO3↓+H+、H++HCO3-=CO2↑+H2O);
(2)乙同学认为有Cu(OH)2生成的理论依据是HCO3-+H2O?H2CO3+OH-、Cu2++2OH-=Cu(OH)2↓;
故答案为:HCO3-+H2O?H2CO3+OH-、Cu2++2OH-=Cu(OH)2↓;
(3)①将沉淀从溶液中分离并净化,应进行过滤、洗涤和干燥等操作,故答案为:过滤;
②为准确测定生成CO2的质量,应防止空气中CO2和水蒸气进入装置,
故答案为:防止空气中CO2和水蒸气进入装置D;
③为减小实验误差,应先通入过量经NaOH处理的空气,排除装置内的二氧化碳气体,即打开K1、K3,关闭K2、K4,通入过量空气,一段时间之后,再关闭K1、K3,打开K2、K4,充分反应,最后还要通入过量经NaOH处理的空气,使生成的二氧化碳全部被吸收,即打开K1、K4,关闭K2、K3,通入过量空气,如若未进行步骤b,将使测量结果偏低,
故答案为:cab; b;
④装置D的质量增加了ng,应为CO2的质量,则m(CuCO3)=
| ng |
| 44g/mol |
| ||
| mg |
| 31n |
| 11m |
故答案为:
| 31n |
| 11m |
点评:本题综合考查物质的含量测定,涉及实验基本操作方法,反应原理探究等知识,题目难度中等,注意从减小实验误差的角度分析,掌握实验基础和物质性质是关键.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
下列反应的离子方程式正确的是( )
| A、钠和硫酸铜溶液反应:2Na+Cu2+=2Na++Cu |
| B、AlCl3溶液中加入足量的氨水制Al(OH)3:Al3++3OH-=Al(OH)3↓ |
| C、向碳酸氢钙溶液中加入过量氢氧化钠溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O |
| D、二氧化硅溶于NaOH溶液:SiO2+2OH-=SiO32-+H2O |
下列仪器:①量筒、②烧杯、③烧瓶、④温度计、⑤容量瓶.在仪器上需要标明使用温度的是( )
| A、①⑤ | B、①④⑤ |
| C、①②④⑤ | D、全部 |
下列有关电解质溶液中微粒的物质的量浓度关系正确的是( )
| A、在0.1 mol?L-1Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-)+c(H2CO3) |
| B、在0.1 mol?L-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
| C、向0.2 mol?L-1NaHCO3溶液中加入等体积0.1 mol?L-1NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
| D、常温下,CH3COONa和CH3COOH混合溶液[pH=7,c(Na+)=0.1 mol?L-1]:c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-) |
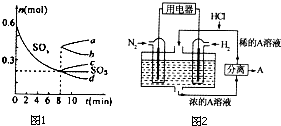 运用化学反应原理研究碳、氮、硫等单质及其化合物的反应有重要意义;
运用化学反应原理研究碳、氮、硫等单质及其化合物的反应有重要意义;