题目内容
根据从草木灰中提取钾盐的实验,填写下列空白:
(1)此实验操作顺序如下:①称量样品,②溶解、沉降,③ ,④ ,⑤冷却、结晶.
(2)用托盘天平(指针向上的)称量样品时,若指针偏向右边,则表示 (填下列正确选项的代码).
A.左盘重,样品轻 B.左盘轻,砝码重C.右盘重,砝码轻 D.右盘轻,样品重
(3)在进行第③步操作时,有可能要重复进行,这是由于 .
(4)在进行第④步操作时,要用玻璃棒不断小心地搅动液体,目的是防止 .
(1)此实验操作顺序如下:①称量样品,②溶解、沉降,③
(2)用托盘天平(指针向上的)称量样品时,若指针偏向右边,则表示
A.左盘重,样品轻 B.左盘轻,砝码重C.右盘重,砝码轻 D.右盘轻,样品重
(3)在进行第③步操作时,有可能要重复进行,这是由于
(4)在进行第④步操作时,要用玻璃棒不断小心地搅动液体,目的是防止
考点:物质分离、提纯的实验方案设计
专题:实验设计题
分析:(1)从草木灰中除去不溶性的固体杂质来提取固体碳酸钾的实验操作顺序为:称量样品,溶解、沉淀,过滤,蒸发浓缩,冷却、结晶;
(2)称量样品时,若指针偏向右边,则砝码的质量偏大;
(3)第③步操作为过滤,多次重复过滤操作,与滤液仍然浑浊有关;
(4)第④步操作为蒸发,应防止局部温度过高.
(2)称量样品时,若指针偏向右边,则砝码的质量偏大;
(3)第③步操作为过滤,多次重复过滤操作,与滤液仍然浑浊有关;
(4)第④步操作为蒸发,应防止局部温度过高.
解答:
解:(1)草木灰中的钾盐可以溶于水中形成溶液,溶解后利用过滤的方法可以获得钾盐的水溶液,将所得的水溶液蒸发浓度、冷却结晶可以获得固体,
故答案为:过滤;蒸发浓缩;
(2)称量样品时,由左物右码的原则可知,若指针偏向右边,砝码质量大,物体质量小,即右盘重,样品轻,故答案为:B;
(3)第③步操作为过滤,多次重复过滤操作,是因为溶液浑浊需多次过滤,故答案为:溶液浑浊需多次过滤;
(4)第④步操作为蒸发,应防止局部温度过高,则用玻璃棒不断小心地搅动液体,目的是防止液体飞溅,故答案为:液体飞溅.
故答案为:过滤;蒸发浓缩;
(2)称量样品时,由左物右码的原则可知,若指针偏向右边,砝码质量大,物体质量小,即右盘重,样品轻,故答案为:B;
(3)第③步操作为过滤,多次重复过滤操作,是因为溶液浑浊需多次过滤,故答案为:溶液浑浊需多次过滤;
(4)第④步操作为蒸发,应防止局部温度过高,则用玻璃棒不断小心地搅动液体,目的是防止液体飞溅,故答案为:液体飞溅.
点评:本题考查混合物分离提纯实验的设计,为高频考点,把握物质的性质及混合物分离方法、基本操作为解答的关键,注意实验基本操作的掌握,题目难度不大.

练习册系列答案
相关题目
用NA表示阿伏加德罗常数的数值,下列说法中正确的是( )
| A、在0.1 mol NaHSO4晶体中阳离子与阴离子总数为0.3 NA |
| B、22.4L NH3中含有的原子总数为4NA |
| C、1mol单质钠在常温下或点燃条件下与O2完全反应转移的电子数都为NA |
| D、常温条件下,等物质的量浓度的HCl溶液和NaOH溶液混合,溶液pH=7 |
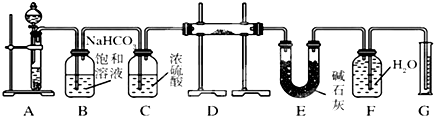
为测定石灰石样品中碳酸钙(含SiO2杂质)的含量.现利用如图所示装置进行实验,充分反应后,测定装置C中生成的BaCO3沉淀质量.下列说法正确的是( )


| A、装置A中药品应为浓硫酸 |
| B、在B-C之间应增添盛有饱和NaHCO3溶液的洗气装置,以除去氯化氢气体 |
| C、为了测得C中生成的沉淀质量,需经过过滤、洗涤、干燥、称量等操作 |
| D、只要测定装置C在吸收CO2前后的质量差,也可以确定碳酸钙的质量分数 |
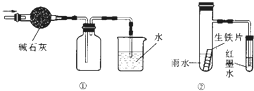
下列有关实验操作或实验原理正确的是( )

| A、提取溴水中的溴,可用加入乙醇萃取的方法 |
| B、用蒸发溶剂的方法将10%的氯化铁溶液变为20%的氯化铁溶液 |
| C、用图 ①的装置可以收集一瓶干燥的氨气 |
| D、用图 ②的装置可以验证生铁片在该雨水中是否会发生吸氧腐蚀 |
某烃的结构简式为 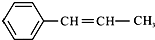 ,它可能具有的性质是( )
,它可能具有的性质是( )
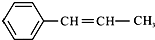 ,它可能具有的性质是( )
,它可能具有的性质是( )| A、能与H2发生加成反应,且需要1 mol H2 |
| B、分子里所有的原子都处在同一平面上 |
C、能发生加聚反应,其加聚产物可用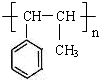 表示 表示 |
| D、该烃和苯互为同系物 |
 已知A、B、C、D是中学化学常见物质,它们在一定条件下有A+B→C+D的转化关系.
已知A、B、C、D是中学化学常见物质,它们在一定条件下有A+B→C+D的转化关系.