��Ŀ����
��10�֣�����������һ��������Ư�������㷺Ӧ����ϴ�·ۡ�Ư�ۡ�ϴ�Ӽ��С�����ɰ(��Ҫ��ΪNa2B4O7)Ϊԭ�������������ƾ������Ҫ�������£�
��1����Na2B4O7��NaOH��Ӧ��NaBO2�����ӷ���ʽΪ �� ��
��2������A�к���������������þ���ʣ�Ϊ�˷����������þ���ڳ����мӹ������ᣬ���˵õ���Mg2+����Һ��������Һ�����ʹMg2+�γ�������þ�����Ӽ�ǰ��Һ��c(Mg2+) ��0.056 mol•L-1����ô�������Һ��pH �� �� ʱ���ſ�ʼ���ֳ�����[��֪25����Mg(OH)2��Ksp��5.6��10��12]
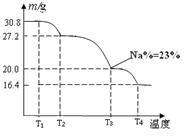
��3����֪��Ʒ�������ƾ����и�Ԫ�ص����ʵ�����Ϊ��n(Na):n(B): n(H) :n(O)=1: 1: n: 7�����ƵõĴ�Ʒ��Ʒ��70�����ϼ��Ƚ���ʧȥ�ᾧˮ����ô�Ʒ�������¶ȵı仯��ͼ��ʾ����T3ʱ���þ���Ļ�ѧʽΪ___��___������д������̣�
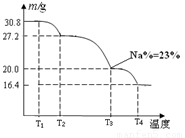
��4������Ӧ�¶ȿ��Ʋ��������õĹ������ƾ����н�����NaBO2 �����Ʒ���Ƶ��������� �� ���� �����ߡ��������͡����䡱���� [��Դ:ZXXK]
��ÿ��2�֣���10�֣���1��B4O72- + 2OH- = 4BO2- + H2O ��2�֣�
��2��pH ��9 ��2�֣�
��3��NaBO3��H2O ����ѧʽ2�֣�����2�֣���4�֣�
������̣�T3ʱ��nNa=��20.0g��23%��/23g.mol-1=0.2mol ��1�֣�
��30.8g��Ʒ�У�nNa:nB:nH:nO=0.2:0.2:0.2n:1.4
��0.2��23+0.2��11+0.2n+1.4��16=30.8
���n=8 ��ԭ����Ϊ��NaBO3��4H2O (1��)
��һ������T3ʱ���þ�������Ԫ�ص���������������ᾧˮ��ĿΪ1 ��
����T3ʱ���þ���Ļ�ѧʽΪNaBO3��H2O ��2�֣�
��4������ ��2�֣�
��������





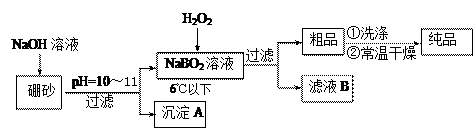
 ���н�����NaBO2 �����Ʒ���Ƶ��������� �� ���� �����ߡ��������͡����䡱����[��Դ:ѧ����ZXXK]
���н�����NaBO2 �����Ʒ���Ƶ��������� �� ���� �����ߡ��������͡����䡱����[��Դ:ѧ����ZXXK]
